选择题
下列物质中属于碱性氧化物的是( )
- A、 SO2
- B、 CaO
- C、 CO
- D、 NaOH
配制一定物质的量浓度的溶液不需要用到的仪器是( )
- A、
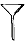
- B、
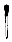
- C、
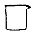
- D、
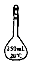
下列物质的水溶液能导电,但属于非电解质的是( )
- A、 Cl2H22O11
- B、 SO3
- C、 NaHCO3
- D、 Br2
化学反应2Na+2CH3CH2OH→2CH3CH2ONa+H2↑的反应类型是( )
- A、 化合反应
- B、 分解反应
- C、 置换反应
- D、 复分解反应
下列物质的水溶液因水解呈碱性的是( )
- A、 NH4Cl
- B、 MgSO4
- C、 KOH
- D、 NaClO
位于元素周期表中第二周期IVA族的元素是( )
- A、 碳
- B、 氧
- C、 硅
- D、 硫
下列说法不正确的是( )
- A、 氢氧化铁胶体可用于净水
- B、 镁合金可用于制造导弹、飞机的部件
- C、 石灰石﹣石膏法可用于燃煤的脱硫
- D、 焦炭在炼铁高炉中用于直接还原铁矿石
下列表示不正确的是( )
- A、 MgF2的电子式:

- B、 二甲醚的结构式:CH3﹣O﹣CH3
- C、 NH3的球棍模型:

- D、 氧原子的结构示意图:

关于硫及其化合物说法正确的是( )
- A、 自然界的硫元素主要以硫单质、硫化物和硫酸盐等形式存在
- B、 浓硫酸可作干燥剂,但不能干燥二氧化硫、氯气等气体
- C、 二氧化硫能使溴水褪色,说明其具有漂白性
- D、 浓硫酸中存在的主要是硫酸分子,常温下就能和铜片剧烈反应
下列说法不正确的是( )
- A、 12C与14C为不同核素
- B、 石墨和C60的互为同素异形体
- C、 H2O和D2O互为同位素
- D、 氨基酸分子中均含有羧基(﹣COOH)和氨基(﹣NH2)
下列说法不正确的是( )
- A、 漂白粉在空气中易变质,所以应密封保存
- B、 工业上可用铁质容器存放浓硫酸
- C、 液氯可储存在钢瓶中,便于运输和使用
- D、 硅酸钠的水溶液俗称“水玻璃”,可保存在带玻璃塞的细口瓶中
在5mL0.1mol•L﹣1KI溶液中滴加0.1mol•L﹣1FeCl3溶液1mL,充分振荡后,再进行下列实验,其中可证明该反应有一定限度的实验是( )
- A、 再滴加AgNO3溶液,观察是否有AgI沉淀产生
- B、 加入CCl4振荡后,观察下层液体颜色
- C、 加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察是否出现红色
- D、 加入CCl4振荡后,取上层清液,滴加入AgNO3溶液,观察是否有AgCl沉淀产生
下列说法不正确的是( )
- A、 生物质能来深于植物及其加工产品所贮存的能量,直接燃烧是利用方式之一
- B、 石油的裂化与裂解都是化学变化,而煤的气化与液化是物理变化
- C、 用高压氢气、氧气制作燃料电池是氢能源利用的一种重要方式
- D、 化学反应过程中反应物的总能量小于生成物的总能量,往往伴随热量的吸收
下列离子方程式正确的是( )
- A、 氯碱工业中电解饱和食盐水:2Cl﹣+2H2O
H2↑+Cl2↑+2OH﹣
- B、 氯化铁溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+
- C、 氢氧化钠溶液吸收少量二氧化硫SO2+OH﹣=HSO3﹣
- D、 稀硫酸中加氢氧化钡溶液至中性:Ba2++H++OH﹣+SO42﹣=BaSO4↓+H2O
如图为元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法不正确的是
![]() ( )
( )
- A、 W的氢化物比R的氢化物稳定
- B、 T的最高价氧化物水化物可能为强碱
- C、 Q的原子半径比T的小
- D、 W和Q的原子序数相差10
下列说法不正确的是( )
- A、 乙烯能使酸性高锰酸钾溶液褪色,发生了氧化反应
- B、 苯在一定条件下能与浓硝酸反应得到硝基苯,发生了取代反应
- C、 乙醛在一定条件与氢气反应生成乙醇,发生了还原反应
- D、 鸡蛋清溶液中加入饱和硫酸铵溶液、饱和硫酸铜溶液均会发生盐析而凝聚
如图是镁一空气燃料电池工作原理示惫图,电池总反应为:2Mg+O2+2H2O=2Mg(OH)2 . 下列有关该电池的说法正确的是( )

- A、 a极为负极,发生还原反应
- B、 b电极上电极反应:O2+2H2O+4e﹣=4OH﹣
- C、 工作时电子由b极经外电路流向a极
- D、 该装置实现了电能转化成化学能
下列说法正确的是( )
- A、 做“钠与水的反应”实验时,切取绿豆粒大小的金属钠,用滤纸吸干表面的煤油,放入烧杯中,滴入两滴酚酞溶液,再加入少量水,然后观察并记录实验现象
- B、 用蒸馏法提纯物质时,如果把温度计水银球位于蒸馏烧瓶支管口下方,会使收集的产品中混有低沸点的杂质
- C、 制备乙酸乙酯时,向乙醇中缓慢加入浓硫酸和冰醋酸,加热3~5min,将导气管插入饱和Na2CO3溶液中以便于除去乙醇和乙酸
- D、 为检验皂化反应进行程度,取几滴反应液,滴入装有热水的试管中,振荡,若有油滴浮在液面上,说明油脂已完全反应
某温度下,在2L密闭容器中投入一定量的A,B发生反应:3A(g)+bB (g)⇌cC(g)△H=﹣Q kJ•mol﹣1(Q>0).12s 时达到平衡,生成C的物质的量为0.8mol,反应过程如图所示.下列说法正确的是( )

- A、 前12s内,A的平均反应速率为0.025mol•L﹣1•s﹣1
- B、 12s后,A的消耗速率等于B的生成速率
- C、 化学计量数之比b:c=1:2
- D、 12s内,A和B反应放出的热量为0.2Q kJ
下列说法不正确的是( )
- A、 CO2、SiO2的晶体结构类型不同
- B、 加热硅、硫晶体使之熔化,克服的作用力不同
- C、 HCl、NaCl溶于水,破坏的化学键类型相同
- D、 NaOH,NH4Cl晶体中既有离子键又有共价键
关于常温下pH均为12的氨水和氢氧化钠溶液,下列说法正确的是( )
- A、 氨水的物质的量浓度等于氢氧化钠溶液
- B、 将氨水体积稀释10倍,pH<11
- C、 等体积氨水和氢氧化钠溶液与足量氯化铁溶液反应,氨水产生的沉淀多
- D、 将等体积的氨水和氢氧化钠用稀盐酸完全中和,消耗盐酸的体积相同
设NA为阿伏加德罗常数的值.下列说法正确的是( )
- A、 1molOH﹣与1mol﹣OH所含质子数均为9NA
- B、 0.1mol/L的CuCl2溶液中含Cl﹣的数目为0.2 NA
- C、 标准状况下,11.2LCCl4中含C﹣C键的数目为2NA
- D、 10 mL2mol/LH2O2完全分解,转移的电子数为0.2 NA
常温下,向20.0mL 0.10mol•L﹣1的NaOH溶液中逐滴加入0.10mol•L﹣1的醋酸溶液,溶液pH随醋酸溶液体积的变化如图所示.下列说法正确的是( )

- A、 N点处恰好完全反应,c(CH3COO﹣)=c(CH3COOH)
- B、 O点处显中性,c(CH3COO﹣)=c(Na+)=c(H+)=c(OH﹣)
- C、 M点到O点过程中,可能出现c(CH3COO﹣)>c(Na+)
- D、 P点处显酸性,c(CH3COO﹣)+c(CH3COOH)=2c(Na+)
已知氧化性:Br2>Fe3+>I2 , 向含a mol FeI2的溶液中加入含b mol Br2的溴水,充分反应.下列说法不正确的是( )
- A、 离子的还原性强弱:I﹣>Fe2+>Br﹣
- B、 当a≥b时,发生的离子反应:2I﹣+Br2═I2+2Br﹣
- C、 当5a=4b时,反应后的离子浓度之比:c(Fe2+):c(Fe3+):c(Br﹣)=1:1:5
- D、 当3a≤2b时,发生的离子反应:2Fe2++2I﹣+2Br2═2Fe3++I2+4Br﹣
某无色溶滚中可能含有Na+、NH4+、Ba2+、Cu2+、SO42﹣、SO32﹣、Cl﹣、Br﹣、CO32﹣中的若干种.为检验其中含有的离子,进行如下实验:
①取10mL溶液,加入足量氯水,.无气体产生,再加入CCl4溶液分层,下层为橙扭色;
②分液后,将①中上层溶液加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448m气体.下列关于原溶液的说法正确的是( )
- A、 肯定存在NH4+、Cl﹣、Br﹣
- B、 SO42﹣、SO32﹣至少含有一种
- C、 是否存在Na+需要通过焰色反应来确定
- D、 肯定不存在Ba2+、Cu2+、SO32﹣、CO32﹣





 +H2O
+H2O