单选题
地壳中含量最多的元素是( )
- A、 Fe
- B、 Al
- C、 Si
- D、 O
下列关于金属的说法中,错误的是( )
- A、 铜有良好的导电性,常用于制作导线
- B、 所有的金属都能与稀盐酸反应
- C、 铁制品在干燥的空气中不易生锈
- D、 不能用铁桶盛放硫酸铜溶液
下列关于资源和能源的叙述中正确的是( )
- A、 目前已制得的纯金属只有90余种,合金已达几百种
- B、 海洋是巨大的资源宝库,海水中含有80多种元素
- C、 现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的40%以上
- D、 地壳中含量最多的金属元素及目前世界年产量最高的金属都是铁
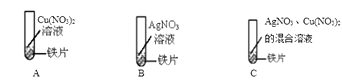
要验证Zn、Cu、Ag三种金属的活动性顺序,同学们设计了以下四个实验。你认为其中不需要进行的是( )
- A、 将锌片放入稀硫酸中
- B、 将铜片放入稀硫酸中
- C、 将铜片放入硝酸银溶液中
- D、 将锌片放入硝酸银溶液中
现有甲、乙、丙三种金属,先将三者分别加入到稀硫酸中,只有乙金属表面有气泡生成;再将甲加入到丙的盐溶液中,无明显变化。据此判断三种金属的活动性由强到弱的顺序是( )
- A、 甲>乙>两
- B、 甲>丙>乙
- C、 乙>丙>甲
- D、 丙>甲>乙
为验证Mg、Fe、Cu三种金属的活动性顺序,所选药品不能达到目的是( )
- A、 Mg、Cu、FeSO4溶液
- B、 Cu、Fe、稀硫酸、MgSO4溶液
- C、 Cu、FeSO4溶液、MgSO4溶液
- D、 Fe、MgSO4溶液、CuSO4溶液
研发高性能“中国芯”是我国信息产业的当务之急。“中国芯”的主要材料是高纯度的单质硅,工业上用SiO2+2C  Si+2CO↑来制取粗硅,下列说法正确的是( )
Si+2CO↑来制取粗硅,下列说法正确的是( )
- A、 生成CO的原因是O2不足
- B、 该反应为置换反应
- C、 硅元素在地壳中的含量比氧元素多
- D、 该反应体现了C的氧化性
根据下面实验装置图,以下说法中正确的是( )

- A、 a处固体由黑色逐渐变为红棕色
- B、 该实验可验证CO的氧化性
- C、 实验结束后应先停止加热,待玻璃管冷却后再停止通CO
- D、 在整个实验过程中,c处的尾气可不做处理直接排放到空气中
如图是探究铁和铜金属活动性实验,关于此实验说法错误的是( )

- A、 铁丝需要砂纸打磨
- B、 溶液由蓝色变为无色
- C、 金属活动性强弱:Fe>Cu
- D、 化学反应方程式为:Fe+CuSO4=Cu+FeSO4
将一定量的金属M加入到含有硝酸锌、硝酸铜、硝酸银的混合溶液中,充分反应后过滤,得到滤渣和滤液,根据实验分析,下列说法正确的是( )
①若滤液为蓝色,则滤渣中一定不含锌和M
②若滤液只含一种溶质,滤渣含四种金属,则几种金属活动性顺序:M>锌>铜>银
③若滤渣含有M,则滤液中的溶质种类最多含3种,最少含一种
④向滤渣中加入稀盐酸产生无色气体,则滤渣中一定含锌,可能含M
- A、 ②④
- B、 ①④
- C、 ②③
- D、 ①③
图中A、B、C、D是立在水田中的电线杆的铁丝拉线的四个部位,其中最容易生锈的是( )

- A、 A处
- B、 B处
- C、 C处
- D、 D处
某兴趣小组在研究Zn-Cu合金、Zn-Fe合金、Fe-Al合金、Fe-Cu合金时,发现其中一种合金6.5g与足量稀盐酸充分反应产生了0.5g气体,该合金可能是( )
- A、 Zn-Cu合金
- B、 Zn-Fe合金
- C、 Fe-Al合金
- D、 Fe-Cu合金