单选题
12.8g氧化铁和氧化铜的混合物与CO充分反应后固体质量减少3.2g,则原混合物中Fe2O3和CuO的质量比为( )
- A、 3:2
- B、 2:1
- C、 3:1
- D、 1:1
将18g高锰酸钾加热,当产生1.6g氧气时,固体剩余物是( )
- A、 KMnO4 MnO2
- B、 K2MnO4 MnO2
- C、 KMnO4 MnO2 K2MnO4
- D、 KMnO4 K2MnO4
在A+3B=2C+2D的反应中,14克A完全反应生成44克C和18克D,若A的相对分子质量为28,则B的 相对分子质量是( )
- A、 16
- B、 32
- C、 64
- D、 96
在化学反应A2+BC=B+A2C中,反应物BC与生成物 B的质量关系如图所示.将2g A2与80g BC恰好完全反应,则生成A2C的质量是( )
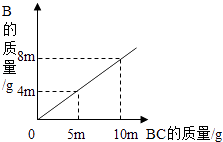
- A、 64g
- B、 18g
- C、 80g
- D、 9g
已知:草钙酸[CaC2O4]比碳酸钙受热易分解,CaC2O4  CaCO3+CO↑.将12.8gCaC2O4固体加热一段时间后剩余7.8g固体.下列说法错误的是( )
CaCO3+CO↑.将12.8gCaC2O4固体加热一段时间后剩余7.8g固体.下列说法错误的是( )
- A、 剩余固体为混合物
- B、 剩余固体中含有钙元素的质量为4.0g
- C、 将剩余固体溶于过量的稀盐酸,产生2.2gCO2
- D、 将加热产生的气体全部通入足量澄清石灰水中,生成10.0g固体
在一密闭容器里放入四种物质,使其在一定条件下充分反应,测得数据如表
四种物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量(g) | 2 | 8 | 30 | 50 |
反应后质量(g) | 20 | 未测 | 39 | 23 |
(已知甲、丙两种物质的相对分子质量之比为1:1)
则下列说法正确的是( )
- A、 该反应为化合反应
- B、 待测值为18
- C、 反应中丁和丙的质量比为3:1
- D、 甲、丙两种物质化学计量数之比为1:2
物质X与Ca(OH)2水溶液发生反应的化学方程式为:X+Ca(OH)2=Y+Cu(OH)2↓,下列说法正确的是( )
- A、 X可能是酸
- B、 X和Y的相对分子质量之差为24
- C、 X可能是单质,也可能是化合物
- D、 Y只可能是CaCl2
为及时发现燃气泄漏,常在燃气中加入少量有特殊气味的乙硫醇(C2H5SH),乙硫醇在煤气燃烧过程中也发生燃烧,其反应如下:2C2H5SH+9O2  4CO2+6H2O+2X,下列关于X的说法正确的是( )
4CO2+6H2O+2X,下列关于X的说法正确的是( )
- A、 X由碳、硫、氧三种元素组成
- B、 X属于有机化合物
- C、 X中硫、氧元素的原子个数比为1:2
- D、 X中氧元素的质量分数为60%
在密闭容器中加入甲、乙、丙、丁四种物质,使之充分反应,反应前后测得有关数据如表:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 18 | 1 | 2 | 32 |
反应后质量/g | X | 26 | 2 | 12 |
下列说法中,不正确的是( )
- A、 反应后物质甲的质量为13g
- B、 乙是反应物
- C、 反应中乙、丁的质量比为5:4
- D、 物质丙可能是该反应的催化剂
10gA和足量B混合加热,充分反应后生成8gC和4gD,则参加反应的A和B的质量比为( )
- A、 1:1
- B、 2:1
- C、 4:1
- D、 5:1
已知:Cu2O+H2SO4═Cu+CuSO4+H2O。16.0g CuO与CO反应得到Cu、Cu2O混合物13.6g,将此混合物溶于足量的100.0g稀H2SO4得9.6gCu.下列说法正确的是( )
- A、 生成2.4g CO2
- B、 混合物中含9.6g铜元素
- C、 混合物中Cu与Cu2O的质量之比为8:9
- D、 反应后溶液中CuSO4的质量分数约为7.0%

