单项选择题
宿迁市城市绿地保护条例经江苏省第十二届人民代表大会常务委员会第二十五次会议,2016年9月30日批准,自2016年12月1日起施行,下列关于绿地作用和保护说法中错误的是( )
- A、 绿地可以保持水土,减少水土流失
- B、 绿地可以调节气候,减少空气中PM2.5含量
- C、 绿地可以吸收二氧化碳,转化生成氧气
- D、 为减少园林绿地中病虫害,大量使用杀虫剂解决问题
下列化学用语的表达正确的是( )
- A、 硫酸的电离方程式:H2SO4=H2++SO42﹣
- B、 光导纤维主要成分的化学式:Si
- C、 质子数为53,中子数为78的碘原子:
I
- D、 钠离子的结构示意图:
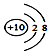
下列关于物质的分类中,正确的是( )
| 酸性氧化物 | 酸 | 盐 | 混合物 | 电解质 |
A | SiO2 | HClO | 烧碱 | KAl(SO4)2•12H2O | C2H5OH |
B | Na2O2 | HNO3 | NaHSO4 | 漂白粉 | Mg |
C | SO3 | H2SiO3 | 纯碱 | 水玻璃 | NaCl |
D | NO | Al(OH)3 | BaCO3 | 铝热剂 | NH3 |
- A、 A
- B、 B
- C、 C
- D、 D
下列氯化物中,既能由金属和氯气直接化合制得,又能由金属和盐酸反应制得的是( )
- A、 CuCl2
- B、 FeCl2
- C、 FeCl3
- D、 NaCl
下列各个反应,不能用于工业生产的是( )
- A、 二氧化锰和浓盐酸共热制氯气
- B、 煅烧黄铁矿(FeS2)制SO2
- C、 氯气与石灰乳反应制漂白粉
- D、 电解熔融氯化镁制金属镁
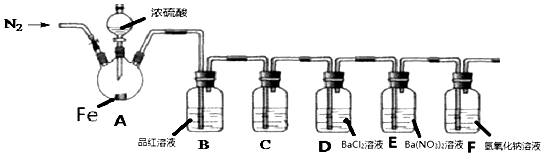
图所示的实验装置图正确且能达到相应实验目的是( )
- A、
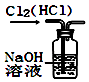 用图所示装置除去Cl2中的HCl
用图所示装置除去Cl2中的HCl - B、
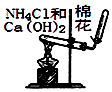 用图所示装置实验室制NH3
用图所示装置实验室制NH3 - C、
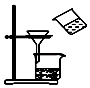 用图所示装置分离MnO2和KCl
用图所示装置分离MnO2和KCl - D、
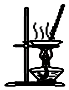 用图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
用图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
下列说法正确的是( )
- A、 常温下可用铁制或铝制容器盛装浓硝酸
- B、 高炉炼铁的主要反应原理是碳在高温下直接将氧化铁还原成铁
- C、 SO2气体可使酸性高锰酸钾溶液褪色,体现了SO2的漂白性
- D、 二氧化碳和二氧化硅都是酸性氧化物,都能与水反应生成相应的酸
与100mL 0.4mol•L﹣1NH4NO3溶液中的NO3﹣浓度相同的是( )
- A、 400 mL 0.1 mol•L﹣1的KNO3溶液
- B、 100 mL 0.4 mol•L﹣1的Ba(NO3)2溶液
- C、 100 mL 0.2 mol•L﹣1的Mg(NO3)2溶液
- D、 200 mL 0.1mol•L﹣1的Fe(NO3)3溶液
下列关于物质用途的叙述中不正确的是( )
- A、 钠和钾的合金可用于快中子反应堆作热交换剂
- B、 FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板
- C、 明矾溶于水后能产生Al(OH)3胶体,可用作净水剂
- D、 在医疗上,可用碳酸钠治疗胃酸过多
一定量CO2通入某浓度的NaOH溶液中,反应后得到溶液A,向A溶液中逐滴滴入某浓度稀盐酸,加入V(HCl)与生成n(CO2)的关系如图所示.下列有关叙述正确的是( )
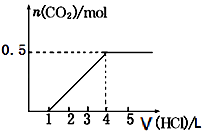
- A、 通入的CO2气体为11.2 L
- B、 A溶液中n(NaHCO3)=2n(Na2CO3)
- C、 A溶液中既含NaOH,又含Na2CO3
- D、 A溶液中一定只有Na2CO3
不定项选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
- A、 FeCl3溶液中:K+、Na+、SO42﹣、SCN﹣
- B、 在强碱性溶液中:K+、Na+、CO3﹣、AlO2﹣
- C、 在盐酸溶液中:K+、Fe2+、SO32﹣、NO3﹣
- D、 与铝反应产生氢气的溶液中:Na+、K+、HCO3﹣、Cl﹣
已知某盐酸、氯化铜、氯化铁的混合溶液100mL,已知溶液中各阳离子物质的量浓度相等,氯离子总物质的量浓度为6mol•L﹣1 , 此溶液中最多可以溶解铁粉的质量为( )
- A、 5.6g
- B、 16.8g
- C、 11.2g
- D、 33.6g