单选题
科学实验要规范操作,下列初中科学实验操作你认为正确的是( )
- A、
 CO2的验满
CO2的验满 - B、
 干燥氧气
干燥氧气 - C、
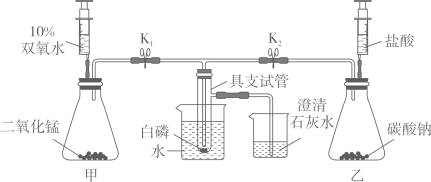
 检验气密性
检验气密性 - D、
 实验室即关即停制取H2
实验室即关即停制取H2
运用图示法可以帮助我们巧学化学。下列化学知识用相应图示表示正确的是( )
- A、
 地壳中各元素质量分数
地壳中各元素质量分数 - B、
 金属活动性
金属活动性 - C、
 含碳量
含碳量 - D、
 硫元素的化合价
硫元素的化合价
我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称LED)技术,已广泛用于照明、显像等多个领域。氮和镓的原子结构示意图及镓在元素周期表中的信息如图所示,下列说法正确的是( )

- A、 氮元素位于第三周期,属于非金属元素
- B、 镓原子核内有31个中子
- C、 镓的相对原子质量是69.72g
- D、 氮化镓的化学式为GaN
小柯为比较Mg、Fe、Cu三种金属的活动性顺序,进行了如图甲所示的实验。实验后把两试管中的物质倒入烧杯中(如图乙),发现烧杯内的红色固体明显增多,充分反应后过滤。滤液中含有的金属离子可能的组成有( )

①Mg2+ ②Mg2+和Fe2+ ③Fe2+和Cu2+ ④Mg2+、Fe2+和Cu2+
- A、 ①②
- B、 ①③
- C、 ②④
- D、 ③④
分析推理是一种重要的化学思维方法,以下推理正确的是( )
- A、 乙醇和甲烷燃烧的产物均为CO2 和H2O,所以二者元素组成一定相同
- B、 化合物中含不同种元素,所以含不同种元素的物质一定是化合物
- C、 化学变化中分子种类发生改变,则分子种类改变的一定是化学变化
- D、 溶液的具有均一性、稳定性,所以均一、稳定的液体一定是溶液
向AgNO3和Mg(NO3)2溶液中加入一定量Zn粉和Cu粉,充分反应后过滤,得到滤渣和蓝色滤液。关于该滤渣和滤液说法正确的是()
- A、 向滤渣中加入稀盐酸,可能有气泡产生
- B、 滤液中一定有Cu(NO3)2、Mg(NO3)2、Zn(NO3)2
- C、 滤渣中一定有Ag,可能有Cu和Zn
- D、 滤液中一定无AgNO3 , 可能有Zn(NO3)2
通过观察下列实验现象,能达到实验目的是( )
- A、
 验证Fe、Cu、Ag的金属活动性强
验证Fe、Cu、Ag的金属活动性强 - B、
 探究溶剂种类对物质溶解性的影响
探究溶剂种类对物质溶解性的影响 - C、
 验证质量守恒定律
验证质量守恒定律 - D、
 探究影响物质溶解速率的因素
探究影响物质溶解速率的因素
以下实验方案设计中,正确的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 除去N2中有少量O2 | 将气体缓缓通过灼热的炭粉 |
| B | 除去CaO中有少量CaCO3 | 加足量的水溶解,过滤 |
| C | 除去CaCl2溶液中的少量盐酸 | 加适量的铁粉 |
| D | 除去CO2中有少量CO | 灼热的CuO |
- A、 A
- B、 B
- C、 C
- D、 D
下列图象能正确反映对应变化关系的是( )
- A、
 AgNO3和Cu(NO3)2的混合溶液中加入锌粉至过量
AgNO3和Cu(NO3)2的混合溶液中加入锌粉至过量 - B、
 等质量镁粉、铁粉中分别加入足量等浓度的稀硫酸
等质量镁粉、铁粉中分别加入足量等浓度的稀硫酸 - C、
 用两份等质量、等浓度的过氧化氢溶液分别制取氧气
用两份等质量、等浓度的过氧化氢溶液分别制取氧气 - D、
 向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉