单选题
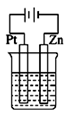
铜制品上的铝质铆钉,在潮湿的空气中易腐蚀的主要原因可描述为( )
- A、 形成原电池,铝作负极
- B、 形成原电池,铜作负极
- C、 形成原电池时,电流由铝流向铜
- D、 铝质铆钉发生了化学腐蚀
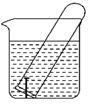
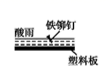
下列情形中,相同材质的铁最不易被腐蚀的是( )
- A、
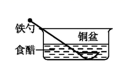
- B、
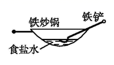
- C、
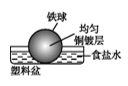
- D、
下列金属防腐的措施中,使用牺牲阳极的阴极保护法的是( )
- A、 地下钢管连接镁块
- B、 金属护栏表面涂漆
- C、 汽车底盘喷涂高分子膜
- D、 水中的钢闸门连接电源的负极
碳钢广泛应用在石油化工设备管道等领域,随着深层石油天然气的开采,石油和天然气中含有的CO2及水引起的腐蚀问题(俗称二氧化碳腐蚀)引起了广泛关注。深井中二氧化碳腐蚀的主要过程如下所示:
负极:Fe(s)+ 2HCO3- (aq) -2e- = FeCO3 (s)+H2CO3(aq)(主要)
正极:2H2CO3(aq) +2e- = H2↑+2HCO3- ( aq)(主要)
下列说法错误的是( )
- A、 钢铁在CO2 水溶液中的腐蚀总反应可表示为CO2+H2O +Fe= FeCO3 +H2
- B、 深井中二氧化碳对碳钢的腐蚀主要为化学腐蚀
- C、 碳钢管道在深井中的腐蚀与油气层中盐份含量有关,盐份含量高腐蚀速率会加快
- D、 腐蚀过程表明含有CO2 的溶液其腐蚀性比相同pH 值的 HCl溶液腐蚀性更强
某小组为研究金属的腐蚀与防护,设计如图所示装置。下列叙述正确的是( )
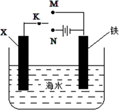
- A、 若X为碳棒,为减缓铁的腐蚀,开关K应置于M处
- B、 若X为碳棒,开关K置于N处,会加快铁的腐蚀
- C、 若X为锌,开关K置于M处,是牺牲阳极的阴极保护法
- D、 若X为锌,开关K置于N处,铁电极发生的反应为:Fe-2e-=Fe3+
下列说法正确的是( )
- A、 Na2O2 在空气中久置,因分解成 Na2O 和 O2 而变成白色固体
- B、 明矾溶于水能形成胶体,可用于自来水的杀菌消毒
- C、 电热水器用镁棒防止内胆腐蚀,原理是牺牲阳极的阴极保护法
- D、 氮气化学性质稳定,可将炽热的镁粉放在氮气中冷却
下列有关电化学在生产、生活中的应用分析正确的是( )

- A、 图1:铁钉发生析氢腐蚀
- B、 图2:可以在铁件上镀铜
- C、 图3:溶液中c(Cu2+)保持不变
- D、 图4:将输油管与电源负极相连可以防止腐蚀
下列有关原电池和金属腐蚀的说法中,不正确的( )
- A、 铜、锌两电极插入稀H2SO4中组成原电池,铜是正极
- B、 原电池中e-从负极流出,负极发生氧化反应
- C、 钢铁的吸氧腐蚀和析氢腐蚀的负极反应均为Fe-3e-=Fe3+
- D、 电化学腐蚀比化学腐蚀更快更普遍
研究性学习小组用如图装置研究钢铁在海水中的腐蚀与防腐,


下列说法正确的是( )
- A、 1中只发生化学腐蚀
- B、 2中发生的是析氢腐蚀
- C、 3为外加电流的阴极保护法
- D、 钢铁被腐蚀的速率: 1>2>3
在下列装置中(都盛有0.1mol·L-1H2SO4溶液)Zn片腐蚀最快的是( )
- A、

- B、
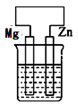
- C、
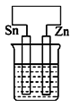
- D、