单选题
下列对于“摩尔”的理解不正确的是( )
- A、 摩尔是一个物理量
- B、 摩尔是物质的量的单位,简称摩,符号为mol
- C、 1mol12C与0.012kg12C所含碳原子数相同
- D、 1molO2约含6.02×1023个氧分子
下列说法中,错误的是( )
- A、 2molH
- B、 1mol H2O
- C、 4mol e﹣
- D、 0.5mol 小米
为了探究FeSO4和Cu(NO3)2的混合物中各组分的含量,现设计如下流程,下列叙述中不正确的是( )

- A、n=0.02
- B、V=2240
- C、 m=3.2
- D、 元混合物中FeSO4的质量分数约为89%
NA为阿伏加德罗常数的值。下列叙述错误的是( )
- A、 1 mol 乙烯分子中含有的碳氢键数为4NA
- B、 1 mol 甲烷完全燃烧转移的电子数为8NA
- C、 1 L 0.1 mol·L−1的乙酸溶液中含H+的数量为0.1NA
- D、 1 mol 的CO和N2混合气体中含有的质子数为14NA
物质的量相等的CO和CO2相比较,下列有关叙述中正确的是( )
①它们所含的分子数目之比为1:1
②它们所含的氧原子数目之比为1:2
③它们所含的原子总数目之比为2:3
④它们所含的C原子数目之比为1:1
⑤它们所含的电子数目之比为7:11.
- A、 ①和④
- B、 ②和③
- C、 ①②③④
- D、 ①②③④⑤
在两个密闭容器中,分别充有质量相等的甲、乙两种气体,它们的温度和密度均相同.试根据甲、乙的摩尔质量(M)的关系,判断下列说法中正确的是( )
- A、 若M(甲)>M(乙),则分子数:甲>乙
- B、 若M(甲)<M(乙),则气体摩尔体积:甲>乙
- C、 若M(甲)<M(乙),则气体的压强:甲>乙
- D、 若M(甲)>M(乙),则气体体积:甲<乙
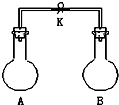
如图所示,室温下,A、B两个容积相等的烧瓶中分别集满了两种气体(同温、同压),当取下K夹,使两烧瓶内气体充分接触后,容器内压强由小到大的顺序正确的是( )
编 号 | ① | ② | ③ | ④ |
A中气体 | H2S | H2 | NH3 | NO |
B中气体 | SO2 | Cl2 | HCl | O2 |
- A、 ②③④①
- B、 ③①④②
- C、 ③②①④
- D、 ④③②①
下列叙述的两个量,一定相等的是( )
- A、 0.1 mol•L﹣1 NaCl与0.05 mol•L﹣1 Na2CO3溶液中的Na+数目
- B、 质量相等的金刚石与C60中的碳原子数目
- C、 标准状况下,等体积的SO2与SO3的分子数目
- D、 28 g乙烯气体和56g环丁烷(C4H8)气体中含有的碳原子数
物质X2CO3的饱和溶液V mL,密度为ρg/cm3 , X+的物质的量浓度为c mol/L,溶质的质量分数为a%,溶质的相对分子量为M,溶质的溶解度为s g.则下列表达式正确的是( )
- A、 c=
×2
- B、 a=
- C、 c=
- D、 V×ρ×a%=
与100mL0.1mol/L AlCl3溶液中Cl﹣的物质的量浓度相等的是( )
- A、 50mL0.1mol/L NaCl溶液
- B、 50mL0.15mol/L MgCl2溶液
- C、 10mL1.0mol/L FeCl3溶液
- D、 100mL0.3mol/L KClO3溶液
设NA为阿伏加德罗常数值,下列说法不正确的是( )
- A、 10 g D216O中所含中子数为5NA
- B、 标准状况下,22.4 L乙烷中所含共价键数目为7NA
- C、 7.8g Na2O2中所含阴、阳离子总数目为0.4NA
- D、 密闭容器中,1 mol N2和3 mol H2充分反应后,容器中的分子数一定大于2NA