单选题
下列气体既有颜色又有毒性的是( )
- A、
- B、
- C、 HCl
- D、
氯气可用来消灭田鼠,为此将氯气通过软管灌入洞中,这是利用了氯气下列性质中的( )
①黄绿色 ②密度比空气大 ③有毒 ④较易液化 ⑤溶解于水
- A、 ②③
- B、 ③④
- C、 ①②③
- D、 ③④⑤
下列为某同学记录的有关氯气的性质及实验现象,其中记录错误的是( )
- A、 氯气是一种有刺激性气味的黄绿色气体
- B、 氯气作用于干燥的pH试纸,试纸不褪色
- C、 纯净的氢气可以在氯气中安静地燃烧,发出苍白色火焰
- D、 红热的铁丝可以在氯气中剧烈燃烧,生成白色的烟
下列化合物不能由单质间的一步反应制得的是( )
- A、 NaCl
- B、 CuCl
- C、 Na2O
- D、 Al2O3
部分常见含氯物质的分类与相应化合价关系如图所示。下列推断不合理的是 ( )

- A、
既可被氧化,也可被还原
- B、
的浓溶液可与
的固体反应生成
与
- C、 实验室可通过加热
与
的浓溶液制得
- D、 可存在
的循环转化关系
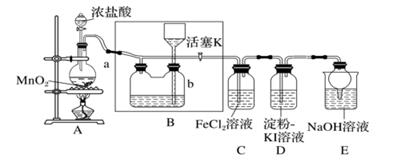
如图所示,将浓盐酸滴在 晶体上生成
晶体上生成 , 立即用表面皿盖好。由实验现象得出的结论正确的是( )
, 立即用表面皿盖好。由实验现象得出的结论正确的是( )

选项 | 实验现象 | 结论 |
A | 滴有酚酞的NaOH溶液褪色 |
|
B | 滴有KSCN的 |
|
C | KI-淀粉溶液变成蓝色 |
|
D | 紫色石蕊溶液先变红后褪色 |
|
- A、 A
- B、 B
- C、 C
- D、 D
下列实验现象的描述正确的是( )
- A、 钠在空气中燃烧,发出黄色火焰,生成白色固体
- B、 氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白雾
- C、 钠在氯气中燃烧,发出黄色火焰,产生淡黄色固体
- D、 铁丝在氯气中燃烧,产生红棕色烟,产物溶于水,溶液呈浅绿色
下列关于氯水的叙述中正确的是( )
- A、 新制氯水中只含有Cl2和H2O两种分子
- B、 新制氯水可以使蓝色石蕊试纸先变红后褪色
- C、 氯气、液氯和氯水是同一种物质
- D、 氯水放置数天后pH变大
人们常用“84”消毒液对环境进行消毒。该消毒液无色,对某些有色物质有漂白作用,对该溶液进行焰色反应,呈黄色。你认为它可能的有效成分是( )
- A、 NaOH
- B、 NaClO
- C、 KMnO4
- D、 Na2CO3
新制氯水中没有的微粒是( )
- A、
- B、
- C、
- D、
下列关于氯气、液氯、新制氯水和久置氯水的叙述正确的是( )
- A、 液氯中存在多种分子和离子
- B、 久置氯水中无HClO
- C、 氯气无漂白性,而液氯有漂白性
- D、 新制氯水和久置氯水均具有漂白性
某同学用下列装置进行有关Cl2的实验。下列说法不正确的是( )

- A、 I图中:实验现象证明氯气无漂白作用,氯水有漂白作用
- B、 II图中:闻Cl2的气味
- C、 III图中:产生苍白色火焰
- D、 IN图中:若气球干瘪,证明Cl2可与NaOH反应
如下图所示,在A处通入未经干燥的氯气.当关闭B阀时,C处的红布条看不到明显现象;当打开B阀后,C处的红布条逐渐褪色.则D瓶中盛放的溶液可能是( )

①饱和NaCl溶液 ②NaOH溶液 ③ ④浓
- A、 ①②
- B、 ①③
- C、 ②④
- D、 ③④
某同学用下图所示装置进行有关Cl2的实验,下列说法错误的是( )

- A、 图Ⅰ中的实验现象能证明氯气无漂白作用,氯水有漂白作用
- B、 用图Ⅱ所示的方法闻Cl2的气味
- C、 图Ⅲ中有棕黄色的烟产生
- D、 图Ⅳ中,若气球干瘪,则可证明Cl2能与NaOH溶液反应
如图所示,  处通入未经干燥的
处通入未经干燥的  ,关闭
,关闭  阀时,C处的红色布条不褪色;打开
阀时,C处的红色布条不褪色;打开  阀时,C处红色布条逐渐褪色。则
阀时,C处红色布条逐渐褪色。则  瓶中装的试剂可能是( )
瓶中装的试剂可能是( )

- A、 浓

- B、 浓盐酸
- C、 H2O
- D、 饱和
 溶液
溶液
某化学兴趣小组为探究干燥的氯气是否具有漂白性,设计如图所示装置进行实验,下列对装置中Ⅰ、Ⅱ、Ⅲ处分别放置的物品判断正确的是( )

| 选项 | Ⅰ | Ⅱ | Ⅲ |
| A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| B | 干燥的有色布条 | 硅胶 | 湿润的有色布条 |
| C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| D | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
- A、 A
- B、 B
- C、 C
- D、 D
氯气及其化合物在生产、生活中应用广泛。实验室常用浓盐酸与 共热[或用
共热[或用 (s)与浓盐酸混合]制取氯气,实验室制取氯气并探究其性质,下列装置不能达到相应实验目的的是 ( )
(s)与浓盐酸混合]制取氯气,实验室制取氯气并探究其性质,下列装置不能达到相应实验目的的是 ( )
A | B | C | D |
|
|
|
|
制取氯气 | 验证氧化性 | 验证漂白性 | 吸收尾气 |
- A、 A
- B、 B
- C、 C
- D、 D
实验室利用如图所示装置制备氯气,图中涉及气体发生、除杂、干燥、收集、尾气处理装置,其中错误的是( )

- A、 ①②③
- B、 ①②④
- C、 ②③④
- D、 ①③④
下列说法正确的是( )
- A、 用
试纸测定某氯水的
为3
- B、 光照氯水有气泡产生,该气体是氯气
- C、 向某溶液中加入硝酸银溶液,产生白色沉淀,则该溶液中一定含氯离子
- D、 在常温下,氯气能溶于水,溶于水中的氯气只有部分与水发生反应