单选题
化学与生活密切相关,下列叙述错误的是( )
- A、 75%的乙醇溶液可以用作医用消毒剂
- B、 铝制餐具用于蒸煮酸性食物
- C、 亚硝酸钠可以用作食品防腐剂
- D、 硅酸钠可以用作黏合剂和防火剂
加碘食盐中的碘以碘酸钾(KIO3)的形式存在。已知在溶液中 与I-可发生反应:
与I-可发生反应: +5I-+6H+=3I2+3H2O。根据上述反应,可用试纸和一些常见试剂进行实验,证明食盐中存在
+5I-+6H+=3I2+3H2O。根据上述反应,可用试纸和一些常见试剂进行实验,证明食盐中存在 。
。
可供选用的物质有:①蒸馏水②蓝色石蕊试纸③碘化钾④淀粉⑤硝酸⑥乙酸⑦乙醇。
进行上述实验时,下列选择正确的是( )
- A、 ①②③⑦
- B、 ①③④⑤
- C、 ①③④⑥
- D、 ①②④⑤⑦
下列变化中,符合图示电子转移的是( )
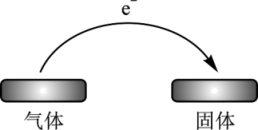
- A、 NH3使CuO变为红色
- B、 CO2使过氧化钠变白
- C、 铝在空气中形成钝化膜
- D、 灼热的铁丝在氯气中燃烧
用如图装置(夹持装置略)进行实验,由b中现象能证明a中产物生成的是( )
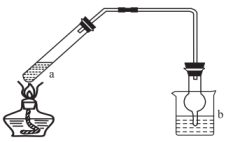
a中反应 | b中检测试剂及现象 | |
A | 铁粉与水生成H2 | 肥皂水冒泡 |
B | 浓NaOH和NH4Cl溶液生成NH3 | 酚酞溶液变红 |
C | 浓HNO3分解生成NO2 | 淀粉—KI溶液变蓝 |
D | 浓HCl与MnO2生成Cl2 | 紫色石蕊溶液变红 |
- A、 A
- B、 B
- C、 C
- D、 D
研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,其主要过程如图所示。
![]()
已知几种物质中化学键的键能如表:
化学键 | H2O中的H-O键 | O2中的O=O键 | H2中的H-H键 | H2O2中的O-O键 | H2O2中的O-H键 |
键能kJ/mol | 463 | 498 | 436 | 138 | 463 |
若反应过程中分解了2mol水,则下列说法错误的是( )
- A、 过程I吸收了926kJ能量
- B、 过程II形成了非极性共价键
- C、 过程III属于放热反应
- D、 总反应为2H2O
2H2↑+O2↑
向盛有少量Na2O2的密闭容器(体积不变)中通入SO2 , 测定容器中O2的含量随时间变化曲线如图,

则下列说法错误的是( )
- A、 ab段O2含量增加的原因:2Na2O2+2SO2=2Na2SO3+O2
- B、 bc段O2含量缓慢降低的可能原因:反应生成O2的速率小于消耗O2的速率
- C、 c点O2含量高于a点,则此时反应产物中含有Na2SO3
- D、 取c点少量固体,加入BaCl2溶液有白色固体生成,证实有Na2SO4生成
一种水性电解液Zn-MnO2电池如图所示(KOH溶液中,Zn2+以Zn(OH) 存在),a、b为离子交换膜。电池放电时,K2SO4溶液的浓度增大。下列叙述错误的是( )
存在),a、b为离子交换膜。电池放电时,K2SO4溶液的浓度增大。下列叙述错误的是( )

- A、 a为阴离子交换膜
- B、 III区的K+通过离子交换b向II区迁移
- C、 I区的H+减少2mol,Zn电极质量减少65g
- D、 电池总反应:Zn+4OH-+MnO2+4H+=Zn(OH)
+Mn2++2H2O
在恒温恒容的密闭容器中,某催化剂表面上发生氨的分解反应:2NH3(g) N2(g)+3H2(g),测得不同起始浓度和催化剂表面积下氨浓度随时间的变化如表所示,下列说法正确的是( )
N2(g)+3H2(g),测得不同起始浓度和催化剂表面积下氨浓度随时间的变化如表所示,下列说法正确的是( )
编号 | 时间/min c(NH3)/(10-3mol•L-1) 表面积/cm2 | 0 | 20 | 40 | 60 | 80 |
① | a | 2.40 | 2.00 | 1.60 | ||
② | a | 1.20 | 0.80 | 0.40 | x | |
③ | 2a | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
- A、 实验①,N2的反应速率:0~20min大于20~40min
- B、 实验②,40min时,v正(NH3)=v逆(NH3)
- C、 相同条件下,增加氨气的浓度,反应速率增大
- D、 相同条件下,增加催化剂的表面积,反应速率增大
将Cl2通入过量石灰乳[Ca(OH)2]中即可制得以Ca(ClO)2为有效成分的漂白粉。下列解释事实的方程式中,错误的是( )
- A、 生成Ca(ClO)2:2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O
- B、 漂白粉溶液与盐酸混合产生Cl2:ClO﹣+Cl﹣+2H+=Cl2↑+H2O
- C、 漂白粉溶液吸收CO2后产生白色沉淀:Ca2++CO2+H2O=CaCO3↓+2H+
- D、 漂白粉溶液加入适量醋酸在短时间内能达到漂白效果:Ca(OH)2+2CH3COOH=Ca(CH3COO)2+2H2O、Ca(ClO)2+2CH3COOH=Ca(CH3COO)2+2HClO
LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工艺流程如图:

已知:BaS易溶于水
下列说法错误的是( )
- A、 还原工序中加入BaS的目的:还原HBr中的少量Br2
- B、 除杂工序中产生滤渣的主要成分为:BaSO4、S
- C、 中和工序中发生的化学反应主要为:Li2CO3+H2SO4=Li2SO4+CO2↑+H2O
- D、 参与反应的n(Br2):n(BaS):n(H2SO4)=1:1:1