选择题(本题共15小题,第1~10小题,每小题4分,第11 ~15小题,每小题3分,共55分。请选出每小题中一个符合题意的选项,不选、错选均不给分)
下列有关安全的说法中正确的是( )
- A、 不慎将氢氧化钠沾到皮肤上,要用大量的水冲洗,再涂上硼酸溶液
- B、 为了方便学习,可将实验室剩余的药品带回家做实验
- C、 工业用盐亚硝酸钠代替食盐烹调食物
- D、 发现家里燃气泄漏,立即打开排气扇
下列用氧化铜制取氢氧化铜的系列操作中正确的是( )
- A、 取用药品

- B、 添加药品

- C、 加快反应

- D、 滴加碱液

将一定量的苯(C6H6)和氧气置于一个完全封闭的容器中引燃,反应生成二氧化碳、水和一种未知物X.测得反应前后物质的质量如下表:列判断正确的是( )
| 物质 | 苯 | 氧气 | CO2 | 水 | X |
| 反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 6.6 | 2.7 | m |
- A、 表中m的值为13.5
- B、 该反应属于分解反应
- C、 物质X能在氧气中燃烧
- D、 物质X中一定含有氢元素
硫酸氢钠(NaHSO4)溶于水为无色溶液,小科预测其化学性质并设计实验验证。下列说法中不正确的是( )
- A、 依据Ba2+与SO42-反应生成BaSO4沉淀,预测NaHSO4能与含Ba2+的盐反应
- B、 向NaHSO4溶液中滴入BaCl2溶液,若有白色沉淀生成,则证明NaHSO4能与含Ba2+的盐反应
- C、 向少量NaOH溶液中滴入NaHSO4溶液,通过观察溶液颜色的变化,验证NaHSO4能与碱反应
- D、 向NaHSO4溶液中滴入Na2CO3溶液,有气泡产生,证明NaHSO4溶液呈酸性
将足量X、Y、Z、M四种金属分别投入等质量、等质量分数的稀盐酸中(如图甲), 把金属Y、Z分别投入硝酸银溶液中( 如图乙),则金属活动性顺序( )

- A、 M>X>Y>Z
- B、 M>X>Z>Y
- C、 X>M>Z>Y
- D、 X>M>Y>Z
想要除去下列物质中的杂质,不正确的是( )
- A、 氮气中混有的少量氧气------将气体通过炽热的铜网
- B、 铜粉中混有的少量氧化铜------加入过量的稀盐酸, 过滤、洗涤、干燥
- C、 氯化钠固体中混有的少量泥沙------溶解,加入硝酸银溶液,过滤
- D、 硫酸锌溶液中混有的少量硫酸铜------加入足量的锌粉,过滤
实验室有四瓶失去标签的无色溶液,分别是碳酸钠溶液、氯化钡溶液、硫酸钠溶液和稀盐酸中的一种。为了鉴别它们,将上述溶液分别标记为甲,乙、丙、丁,做如下实验:各取少许,将甲分别滴加到另外三种溶液中,观察到乙和丁中产生白色沉淀,丙中无明显现象。据此可判断甲是( )
- A、 碳酸钠溶液
- B、 氯化钡溶液
- C、 硫酸钠溶液
- D、 稀盐酸
如图,重力为6N的物体在4N拉力F的作用下,以0.2m/ s的速度沿斜面匀速上升。当物体升高0.6m时,物块恰好沿斜面前进1.2m的距离。忽略绳重和动滑轮自重,则( )

- A、 物体对斜面的压力为6N
- B、 该装置的机械效率为75%
- C、 物体与斜面间的摩擦力为8N
- D、 拉力F的功率为1.6W
某游客来栎社国际机场乘机,他所用的拉杆旅行箱示意图如图所示。装有物品的旅行箱整体可视为杠杆,O为支点,B为重心,A为拉杆的端点。在A点沿图示方向施加拉力F使旅行箱保持静止。下列说法正确的是( )
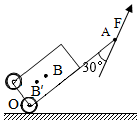
- A、 旅行箱受到的重力与水平地面对它的支持力是一对平衡力
- B、 其他条件不变时,仅缩短拉杆的长度, 拉力F减小
- C、 其他条件不变时,使拉力F的方向沿顺时针改变10°,拉力F增大
- D、 箱内物体下滑,重心位置由B变至B',拉力F增大
如图甲所示,用动滑轮将正方体物块从装有水的容器底部缓慢匀速提起,拉力F随提升高度h变化的关系如图乙所示.物块完全离开水面后,动滑轮的机械效率为87.5%,绳重和摩擦忽略不计。下列选项正确的是( )

- A、 物块的棱长为0.6m
- B、 动滑轮重为300N
- C、 物块完全离开水面前,动滑轮的机械效率大于87.5%
- D、 将物块提升至上表面与水面相平的过程中,拉力F做的功为1650J
向盛有CuSO4和H2SO4混合溶液的烧杯中,逐滴加入NaOH溶液至过量,沉淀质量、溶质质量和溶剂质量随NaOH溶液质量变化关系如右图。下列说法错误的是( )

- A、 乙代表溶质质量
- B、 Q点溶液中溶质为Na2SO4
- C、 O→P过程反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O
- D、 原溶液中CuSO4和H2SO4质量相等
氢能是绿色的能源,如图是制取与贮存氢气的一一种方法。下列说法正确的是( )

资料:①Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金;
②MgH2和HCl反应的化学方程式为MgH2+2HCl=MgCl2+ 2H2↑。
- A、 反应3的基本反应类型是置换反应
- B、 循环制氢反应中需要不断加入ZnO和Fe3O4
- C、 反应3中氩气作保护气,防止金属镁、铜在高温下与氧气反应
- D、 反应3的产物与足量稀盐酸反应生成的氢气和反应2产生的氢气质量相等
天平两边的烧杯中分别装入等质量、等溶质质量分数的稀盐酸,调节天平处于平衡状态,将等质量的CaCO3固体和KHCO3固体分别加入两烧杯中,充分反应后,下列说法正确的是( )
- A、 若天平不平衡,则指针一定偏向加KHCO3的一侧
- B、 若天平不平衡,则两个烧杯中的酸一定都有剩余
- C、 若反应后两烧杯中的固体均有剩余,则天平一定平衡
- D、 若反应后两烧杯中的酸均有剩余,则天平一定平衡
为探究CO2与NaOH溶液发生的反应,某兴趣小组将CO2持续通入一定浓度-定量的NaOH溶液中,用数字化实验技术测定反应过程中溶液的pH和温度变化,结果如图1、图2所示(实验条件下,Na2CO3溶液和NaHCO3溶液的pH分别约为11.0和8.5)。下列说法不正确的是( )

- A、 二氧化碳与氢氧化钠反应放热
- B、 图1中,BC段发生的反应是CO2+Na2CO3+H2O=2NaHCO3
- C、 图1中,pH=12时对应溶液中的溶质只含Na2CO3和NaHCO3
- D、 对于现象不明显的反应,可通过现代技术手段实现反应过程的“可视化”










