单选题
某反应前后分子变化的微观示意图如下,下列说法正确的是( )

- A、 反应有单质生成
- B、 反应前后原子种类、数目不变
- C、 反应物和生成物共有8种物质
- D、 该反应为分解反应
我们在学习物质变化规律时,常用图像来描述化学变化中物质量的变化,下列图线的变化趋势能正确描述对应的实验操作的是( )

- A、 ①向一定量稀硫酸中加入NaOH溶液
- B、 ②向一定量稀硫酸中加入Zn粉
- C、 ③将CO2通入一定量的NaOH溶液
- D、 ④向一定量NaOH和Ca(OH)2的混合溶液中加入Na2CO3溶液
如图所示为小明整理的与氧气化学性质有关的部分笔记,下列关于笔记内容的说法正确的是( )

- A、 都是化合反应
- B、 反应物都是非金属
- C、 都有气体生成
- D、 只有两个是氧化反应
杭州正在创建文明城市,以下做法提倡的是( )
- A、 聚餐时使用公勺公筷
- B、 使用冷空调时把温度降到最低
- C、 将废旧电池丢入其他垃圾桶
- D、 化工厂加高烟囱排放废气,防止酸雨形成
化学兴趣小组利用如图所示的改进装置测定空气中氧气的含量。胶头滴管中的水接触生石灰一段时间后, 白磷开始燃烧, 待白磷熄灭冷却至室温后打开弹簧夹。下列关于该实验的说法错误的是( )

- A、 白磷不足会使测定结果偏小
- B、 注射器活塞会先向左再向右最终停在 10mL 刻度处
- C、 白磷燃烧的过程中会产生大量白烟
- D、 胶头滴管中的水和注射器中的水作用是不相同的
实验室测定蜡烛在盛有一定体积空气的密闭容器内燃烧至熄灭过程中,O2和CO含量随时间变化曲线如图,通过分析该图可推理出的结论是( )

- A、 曲线①表示CO含量的变化
- B、 蜡烛熄灭时,容器内氧气耗尽
- C、 蜡烛由碳、氢元素组成
- D、 蜡烛发生了不完全燃烧
某化学反应的反应物和生成物的微观示意图及反应前后的质量如下表所示:
| 物质 | 甲 | 乙 | 丙 | 丁 | |
| 微观示意图 | | | | | |
| 反应前质量/g | 32 | 200 | 1 | 0 | |
| 反应后质量/g | 0 | x | y | z |
下列有关该反应的说法正确的是( )
- A、 甲物质由碳原子和氢原子直接构成
- B、 该反应属于置换反应
- C、 参加反应的反应物分子个数比为1: 1
- D、 x+y+z= 233
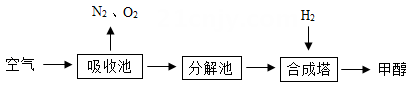
6月5日是世界环境日,2022年世界环境8的主题是“共建清洁美丽的世界”。下列措施会引起环境污染的是( )
- A、 将煤脱硫后再综合利用
- B、 用人畜粪便等废弃物制得甲烷作燃料
- C、 直接焚烧生活垃圾
- D、 大力推广使用太阳能、风能等绿色能源
实验室制取CO2气体的有关操作如下图,正确的是( )
- A、 检查气密性

- B、 制取气体

- C、 收集

- D、 验满

在密闭容器中有甲、乙、丙、丁四种物质在一定条件下反应,测得反应前及反应过程中的两个时刻各物质的质量分数如图所示。图中a、b、c、d分别表示相应物质的质量分数。下列说法正确的是( )

- A、 乙可能是催化剂
- B、 丁是反应物
- C、 甲和乙是反应物
- D、 乙是生成物
如图是探究反应前后质量变化的实验,玻璃管在酒精灯上烧热后,塞紧橡皮塞的同时玻璃管触碰瓶底的白磷,白磷燃烧。下列说法正确的是( )

- A、 反应结束后,瓶内物质的总质量减少
- B、 白磷燃烧时锥形瓶内有大量白烟生成
- C、 玻璃管顶端气球的体积先变小再变大
- D、 实验中反应的化学方程式为:S+O2=SO2