选择题
甲~戊均为短周期元素,在元素周期表中的相对位置如图2所示;戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是( )
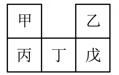
- A、 原子半径:丁>戊>乙
- B、 非金属性:戊>丁>丙
- C、 甲的氢化物遇氯化氢一定有白烟产生
- D、 丙的最高价氧化物对应的水化物一定能与强碱反应
常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为 )的pH和原子半径、原子序数的关系如图所示。下列说法正确的是
)的pH和原子半径、原子序数的关系如图所示。下列说法正确的是
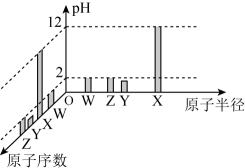
- A、 第一电离能:
- B、
含有极性共价键和非极性共价键
- C、 工业上通过电解XZ的水溶液来制取X的单质
- D、 Z的单质具有强氧化性和漂白性
高铁酸钾( )是一种环保、高效、多功能饮用水处理剂,在水处理过程中,高铁酸钾转化为
)是一种环保、高效、多功能饮用水处理剂,在水处理过程中,高铁酸钾转化为 胶体,下列说法不正确的是
胶体,下列说法不正确的是
- A、 高铁酸钾中铁元素的化合价为+6价
- B、 Fe元素位于周期表ds区
- C、 高铁酸钾属于强电解质
- D、 用
对饮用水处理时,能起到消毒杀菌和吸附杂质的双重作用
一种麻醉剂的结构式如图所示。元素X的原子核只有1个质子,元素Y 、Z、W的原子序数依次增大,且均位于X的下一周期,元素E的原子比元素W的原子多8个电子。下列说法错误的是

- A、 Y的简单氢化物沸点比Z的低
- B、 简单离子半径:Z>W>E
- C、 ZW2中,Z的化合价为+2价
- D、 X、Z、E能形成具有漂白性的化合物
X、Y、Z为原子序数依次增大的主族元素,Y与Z同主族。W为第四周期元素,最外层电子数为1,价层电子数为11,四种元素组成的某蓝色晶体基本结构单元的结构简式如下图所示。下列说法错误的是

- A、 原子半径Z>Y>X
- B、 Y的第一电离能比同周期相邻元素小
- C、 单质W和Z在加热条件下生成化合物WZ
- D、 Y的简单氢化物的热稳定性强于Z的简单氢化物
一种钠盐的结晶水合物的阴离子由短周期元素X、Y、Z组成,其结构如图,已知:Z为第二周期元素,三种元素原子序数之和小于20,下列说法正确的是
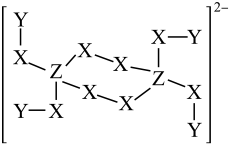
- A、 X、Y、Z三种元素中原子半径最大的是X
- B、 NaZY4是一种强还原剂,其固体溶于水可产生Y2
- C、 Z原子的L层上有5个电子
- D、 X的氢化物中不可能存在非极性共价键
下列物质性质的变化规律与化学键强弱无关的是
- A、 HF、HCl、HBr的热稳定性依次减弱
- B、 NaF、NaCl、NaBr的熔点依次降低
- C、 Li、Na、K的熔点逐渐降低
- D、 SiF4、SiCl4、SiBr4的熔、沸点逐渐升高
X、Y、Z、W、R五种前20号主族元素,原子序数依次增大。基态X原子中有3个未成对电子,Z是元素周期表中电负性最大的元素,Y和W同主族,常温下 的最高价氧化物对应的水化物溶液的pH=12。下列说法正确的是
的最高价氧化物对应的水化物溶液的pH=12。下列说法正确的是
- A、 简单离子半径:r(W)<r(R)
- B、 最高正价:X<Y<Z
- C、 第一电离能:
- D、 简单氢化物的键角:Y>W
短周期元素X、Y、Z、W的原子序数依次增大,Z是地壳中含量最多的元素,W的单质常温下是黄绿色气体。由这四种元素组成的化合物A是一种重要的脱氢剂,化合物A与氢气反应可以生成化合物B,其过程如图所示。下列说法错误的是

- A、 工业上可采用电解饱和食盐水的方法制备W的单质
- B、 Y的最高价氧化物的水化物是强电解质
- C、 Y、Z与氢三种元素形成化合物的晶体类型一定是分子晶体
- D、 用FeCl3溶液可鉴别A和B
氨硼烷(BH3NH3)分子结构和乙烷相似,是一种固体储氢材料。下列关于氨硼烷的说法错误的是
- A、 N和B元素均位于元素周期表的p区
- B、 第一电离能:N<B
- C、 分子中N原子与B原子间形成了配位键
- D、 氨硼烷固态时为分子晶体
- A、 第一电离能:
- B、 原子半径:Se<As
- C、 还原性:
- D、 沸点:
X、Y、Z、W四种短周期元素在周期表中的位置如图所示,X元素基态原子的最外层电子排布式为 。下列说法错误的是
。下列说法错误的是
X | ||
Y | Z | W |
- A、 离子半径:
- B、 还原性:
- C、 酸性:
- D、 氢化物稳定性:
短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X基态原子的p轨道处于半充满状态;常温下,Y的氢化物呈液态,Z的单质能溶于W的最高价氧化物对应的水化物的稀溶液,却不溶于其浓溶液。下列说法错误的是
- A、 第一电离能:
- B、 氢化物的热稳定性:
- C、 电负性:
- D、 原子半径:
化学与科技、生产生活等各方面息息相关,下列说法错误的是
- A、 Ge的单晶可以作为光电转换材料用于太阳能电池
- B、 2022冬奥部分场馆建筑应用了新材料碲化镉发电玻璃,其中碲和镉均属于过渡元素
- C、 牙膏中添加的SrF2、NaF提供的氟离子浓度相等时,它们防治龋齿的作用相当
- D、 冬天前用石灰浆喷洒树皮可以杀死虫卵
短周期主族元素W、X、Y、Z的原子序数依次增加。K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体。K是无色气体,是主要的大气污染物之一。0.1mol/L丙溶液的pH<1,上述物质的转化关系如图所示。下列说法正确的是

- A、 丙不能由无单质参加的化合反应制得
- B、 K、L、M中键角大小为:K>L>M
- C、 元素的非金属性:Z>Y>X
- D、 W、X、Y、Z可形成四种常见的具有漂白性的单质或化合物,包含了三种漂白原理
已知X、Y、Z、W为核电荷数依次增大的前20号主族元素,且位于不同周期,其形成的某种物质的结构如图,该物质的水溶液显酸性。下列说法正确的是

- A、 该化合物的焰色试验呈黄色
- B、 Z的简单气态氢化物的热稳定性比Y强
- C、 Z的最高价氧化物对应的水化物为强酸
- D、 Y与其他三种元素均可形成两种或两种以上的二元化合物
一研发团队基于
 型异质结的
型异质结的 、
、 、
、 的超痕量同时检测及其机理如图所示。下列叙述错误的是
的超痕量同时检测及其机理如图所示。下列叙述错误的是

- A、 图中涉及的金属元素位于元素周期表d区
- B、 图中含金属的纯净物为单质或氧化物
- C、 上述涉及的四种金属元素均为过渡元素
- D、 炭粒在制备氧化物的过程中表现氧化性
上海科研团队发现M是感知各种代谢活动的关键枢纽。M的结构如图所示。短周期主族元素R、Y、Z、X的原子半径依次减小,R为金属元素,X和R位于同主族,Y与R不同周期。下列叙述正确的是

- A、 简单离子半径:
- B、
能与
溶液反应
- C、 Z和R组成的化合物
只含1种化学键
- D、 工业上电解熔融的
制备
的单质
下列符号表征或说法错误的是( )
- A、 氨的电子式:
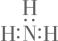
- B、 Cu位于元素周期表的ds区
- C、
在水中的电离方程式:
- D、
的VSEPR模型:

物质M是N−甲基−D−天冬氨酸受体的变构调控因子,其结构式如图所示。其中X、Y、Z、W、R为核电荷数依次增大的短周期主族元素。X的族序数与周期数相等,且与R同主族,Y形成的化合物种类最多。下列说法正确的是

- A、 原子半径:Y>Z>W>R
- B、 简单氢化物沸点:W>Z>Y
- C、 Z2X4中只含有极性共价键
- D、 W、R形成的二元化合物均有强氧化性
已知某化合物的结构如图所示,其中X、Y、Z和W是原子序数依次增大的短周期元素,Y与W是同一主族元素。下列说法正确的是

- A、 原子半径:r(X)>r(Y)>r(Z)>r(W)
- B、 简单氢化物的沸点:Y>Z
- C、 该化合物中各原子均达到8电子稳定结构
- D、 氧化物的水化物的酸性:X>W
前四周期元素W、X、Y、Z的原子序数依次增大且分属不同周期。X的最高能级的电子数比电子层数多1,Y的最高价含氧酸为具有吸水性的弱酸,Z与W中均存在单电子,且两者单电子数和最外层电子数均相同。下列说法正确的是
- A、 四种元素中电负性最大的为Y
- B、 X元素的第一电离能高于其同周期相邻元素
- C、 Z元素在同周期中金属性最强
- D、 W与X两种元素形成的化合物中只含有极性键
硒化锌 是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为该晶胞沿z轴方向在
是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为该晶胞沿z轴方向在 平面的投影,已知晶胞边长为
平面的投影,已知晶胞边长为 , 阿伏加德罗常数的值为
, 阿伏加德罗常数的值为 , 下列说法错误的是
, 下列说法错误的是

- A、
位于元素周期表的
区
- B、 基态
原子核外有18种不同空间运动状态的电子
- C、 A点原子的坐标为
, 则B点原子的坐标为
- D、 该晶体密度为
X、Y、Z、M为原子序数依次增大的前四周期元素,其有关性质或结构信息如下:
元素 | X | Y | Z | M |
性质或结构信息 | 原子核外有三个能级,每个能级含有的电子数都相等 | 原子核外有两个电子层,最外层有3个未成对电子 | 氢化物为二元弱酸 | 基态原子核外价电子排布式为 |
下列说法错误的是
- A、 X元素与Z元素的原子可构成直线形分子
- B、 Y元素氢化物的沸点一定比X元素氢化物的沸点高
- C、 Z元素的二价阴离子
是正四面体结构
- D、 将M的低价硝酸盐溶解在足量稀硝酸中,有气体产生
下列我国科研成果所涉及的物质转化中,物质所含元素位于0族的是( )
- A、 由二氧化碳制取汽油:
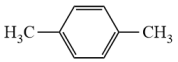 等
等 - B、 液氦到超流氦的转变:液氦(-269℃)→超流氦(-271℃)
- C、 煤炭的清洁化利用:煤炭→
- D、 利用太阳能合成燃料:
下图为某物质的结构。已知:W、Y、Z属于不同周期、不同主族的短周期元素,W、Y、Z原子最外层电子数之和等于X原子最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述错误的是( )
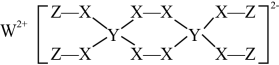
- A、 Y元素在周期表中的位置为第二周期IVA族
- B、 W、X对应的简单离子半径:X>W
- C、 该物质具有强氧化性,可以用作漂白剂
- D、 该物质中,Y、X原子的最外层均满足8电子结构
一种新型漂白剂(如图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述正确的是( )

- A、 W单质在空气中点燃发出耀眼的白光
- B、 W、X对应的简单离子半径W>X
- C、 Y的单质高温下可与水反应放出氢气,体现Y的氧化性
- D、 该漂白剂的漂白原理与
相同
X、Y、Z、M、W是五种短周期主族元素,其原子半径与原子序数的关系如图甲所示,X、Y、Z、M形成的化合物如图乙所示,Z与W同主族。下列说法错误的是( )
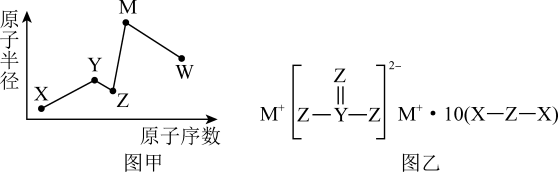
- A、 简单氢化物的熔沸点:Z>W
- B、 简单离子的半径:W>Z>M
- C、 X2Z2和M2Z2中的化学键类型完全相同
- D、 最高价氧化物对应水化物的酸性:W>Y
X、Y、Z为前10号原子序数递增的同周期紧邻元素,基态Z原子的第一电离能的大小在本周期元素中排第二位。下列说法错误的是( )
- A、 电负性:X>Y>Z
- B、 基态原子未成对电子数:X>Y>Z
- C、 原子半径:X>Y>Z
- D、 简单气态氢化物稳定性:Z>Y>X

