选择题
甲基叔丁基醚(MTBE)是一种高辛烷值汽油添加剂,可由甲醇和异丁烯(以IB表示)在催化剂作用下合成,其反应过程中各物质相对能量与反应历程的关系如图所示(其中 表示甲醇和异丁烯同时被吸附,
表示甲醇和异丁烯同时被吸附, 表示甲醇先被吸附,
表示甲醇先被吸附, 表示异丁烯先被吸附),下列说法错误的是
表示异丁烯先被吸附),下列说法错误的是

- A、 三种反应历程中,
反应速率最快
- B、 该条件下反应的热化学方程式为:
- C、 甲醇比IB更易被催化剂吸附,所以若甲醇过多会占据催化剂表面从而减慢合成速率
- D、 同温同压下,只要起始投料相同,相同时间三种途径MTBE的产率一定相同
下图是用钌 基催化剂催化
基催化剂催化 和
和 的反应示意图,当反应生成
的反应示意图,当反应生成 液态
液态 时放出
时放出 的热量。下列说法错误的是
的热量。下列说法错误的是

- A、 反应历程中存在极性键、非极性键的断裂与形成
- B、 图示中物质I为该反应的催化剂,物质II、III为中间产物
- C、 使用催化剂可以降低反应的活化能,但无法改变反应的焓变
- D、 由题意知:
以乙炔和1,2-二氯乙烷为原料生产氯乙烯包括如下反应:
反应I:ClCH2CH2Cl(g)→HCl(g)+CH2=CHCl(g) ΔH1=+69.7 kJ•mol-1
反应Ⅱ:HC≡CH(g)+HCl(g)→CH2=CHCl(g) ΔH2=-98.8 kJ•mol-1
1.0×105Pa下,分别用如表三种方式进行投料,不同温度下反应达到平衡时相关数据如图所示。| 方式 | 气体投料 | 平衡时相关数据 |
| 甲 | ClCH2CH2Cl | ClCH2CH2Cl转化率 |
| 乙 | n(HC≡CH):n(HCl)=1:1 | HC≡CH转化率 |
| 丙 | n(ClCH2CH2Cl):n(HC≡CH)=1:1 | CH2=CHCl产率 |

下列说法错误的是
- A、 反应ClCH2CH2Cl(g)+HC≡CH(g)→2CH2=CHCl(g)的ΔH=-29.1 kJ•mol-1
- B、 曲线①表示平衡时ClCH2CH2Cl转化率随温度的变化
- C、 按方式丙投料,其他条件不变,移去部分CH2=CHCl可能使CH2=CHCl的产率从X点的值升至Y点的值
- D、 在催化剂作用下按方式丙投料,反应达到平衡时CH2=CHCl的产率(图中Z点)低于X点的原因可能是催化剂活性降低
设 为阿伏加德罗常数的值。接触法制备硫酸的原理:(1)
为阿伏加德罗常数的值。接触法制备硫酸的原理:(1) ;(2)
;(2) ;(3)
;(3) 。下列说法正确的是
。下列说法正确的是
- A、
的硫酸溶液中含
的数目为
- B、 反应(2)中
和
反应放出
热量时生成
分子的数目为
- C、
, 则
- D、 反应(1)中生成
转移的电子数为
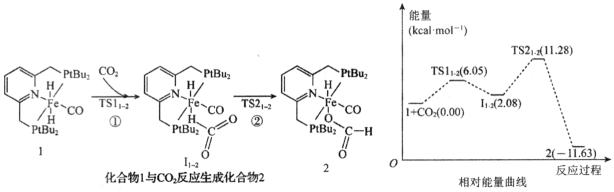
下图是我国科研工作者研究 与
与 作用最终生成
作用最终生成 与
与 的物质相对能量-反应进程曲线。下列叙述错误的是
的物质相对能量-反应进程曲线。下列叙述错误的是

- A、 中间体
比
更稳定
- B、 该反应进程中的最大能垒(活化能)为
- C、 生成
的过程中有极性键的断裂和形成
- D、 总反应的热化学方程式为
②
下列说法错误的是
- A、 液态水变为水蒸气破坏的是分子间作用力
- B、 水分解为氢气和氧气,断键吸收的总能量大于成键放出的总能量
- C、 标准状况下,
水中含共用电子对总数约为
- D、
、
下,
Ni可活化C2H6制得CH4 , 其反应历程如图所示:

下列关于活化历程的说法正确的是( )
- A、 中间体2→中间体3的活化能小于中间体1→中间体2
- B、 Ni在该反应中作催化剂
- C、 可以用焓判据来判断该反应是否自发进行
- D、 Ni(s)+C2H6(g)=NiCH2(s)+CH4(g) ΔH=+6.57kJ·mol-1
CO2催化加氢合成二甲醚是一种CO2转化方法,其过程中主要发生下列反应:
反应I:CO2(g)+H2(g) =CO(g)+H2O(g) ΔH=+41.2 kJ·mol−1
反应II:2CO2(g)+6H2(g) =CH3OCH3(g)+3H2O(g) ΔH=-122.5 kJ·mol−1
在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图所示。 (CH3OCH3的选择性=×100%)

下列说法错误的是( )
- A、 CO的选择性随温度的升高逐渐增大
- B、 反应2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g) ΔH=-204.9 kJ·mol−1
- C、 在240~320℃范围内,温度升高,平衡时CH3OCH3的物质的量先增大后减小
- D、 反应一段时间后,测得CH3OCH3的选择性为48%(图中A点),增大压强可能将CH3OCH3的选择性提升到B点
已知2H2(g)+O2(g)=2H2O(g)+483.6kJ。下列说法正确的是( )
- A、 1mol氢气完全燃烧生成液态水放出的热量小于241.8KJ
- B、 1mol水蒸气完全分解成氢气与氧气,需吸收241.8kJ热量
- C、 2mol氢气与1mol氧气的总能量小于2mol 水蒸气的总能量
- D、 2mol氢氢键和1mol氧氧键拆开所消耗的能量大于4mol氢氧键成键所放出的能量
CO2还原为甲醇是人工合成淀粉的第一步。CO2催化加氢主要反应有:
反应I.CO2(g)+ 3H2(g)=CH3OH(g)+H2O(g) △H1= - 49.4 kJ·mol-1
反应Ⅱ.CO2(g)+H2(g)=CO(g)+ H2O(g) △H2=+41.2 kJ ·mol-1
压强分别为p1、p2时,将 =1:3的混合气体置于密闭容器中反应,不同温度下体系中CO2的平衡转化率和CH3OH、CO的选择性如图所示。CH3OH(或CO)的选择性=

下列说法正确的是( )
- A、 反应CO(g)+ 2H2(g)= CH3OH(g) △H= -8.2 kJ·mol-1
- B、 曲线③、④表示CO的选择性,且pl>p2
- C、 相同温度下,反应I、Ⅱ的平衡常数K(I)>K(Ⅱ)
- D、 保持反应温度不变,使CO2的平衡转化率达到X点,改变的条件可能是增大
或增大压强
ICl与H2能发生的总反应为H2(g)+2ICl(g)=I2(g)+2HCl(g) △H<0。
已知:①该反应分两步完成,第一步为
②两步反应的活化能分别为Ea1、Ea2 , 且Ea1>Ea2
下列判断正确的是( )
- A、 总反应中I2为氧化产物
- B、 第一步的化学反应速率大于第二步的化学反应速率
- C、 已知键能:
,可推知键能H-Cl<I-Cl
- D、 第二步的化学方程式可能为
对于反应4HCl(g)+O2(g) 2Cl2(g)+2H2O(g),下列说法正确的是( )
2Cl2(g)+2H2O(g),下列说法正确的是( )
- A、 该反应△S>0
- B、 使用催化剂能降低该反应的△H
- C、 反应中每消耗1molO2转移电子数约为4×6.02×1023
- D、 反应的平衡常数为K=
下列方程式与所给事实不相符的是( )
- A、
通入氯水中,溶液褪色:
- B、 酚酞滴入
溶液中变为浅红色:
- C、 冷凝
气体得到
液体:
- D、 制备
时,需除去溶液中的氧气,防止发生:
我国提出了2030年前碳达峰、2060年前碳中和的“双碳”目标。二氧化碳催化加氢合成 是一种实现“双碳”目标的有效方法,其主要反应的热化学方程式为
是一种实现“双碳”目标的有效方法,其主要反应的热化学方程式为
反应Ⅰ:
反应II:
下列说法正确的是( )

- A、 1个固态
晶胞(如上图)中含14个
分子
- B、 反应
- C、 用E表示键能,反应I的
- D、
能与水互溶,主要原因是
与
分子间形成氢键
下图是能量示意图,由此判断热化学方程式正确的是( )

- A、
- B、
- C、
- D、
理论研究表明,在101kPa和298K下,HCN(g)  HNC(g)异构化反应过程的能量变化如图所示。下列说法正确的是 ( )
HNC(g)异构化反应过程的能量变化如图所示。下列说法正确的是 ( )

- A、 HCN和HNC中碳氮键完全相同
- B、 HCN和HNC互为同素异形体
- C、 1molHNC(g)的能量高于1molHCN(g)
- D、 HCN(g)
HNC(g)+59.3kJ
一定条件下氨气和氯气反应的能量与反应过程如图所示,下列说法正确的是( )

- A、 相同条件下Cl2比HCl稳定
- B、 过程I:断裂极性键和非极性键
- C、 过程Ⅱ:形成极性键和非极性键
- D、 热化学方程式为NH3(g)+Cl2(g)→NH2Cl(g)+HCl(g) △H=+11.3KJ
 (g) ΔH2=-267.80kJ·mol-1
(g) ΔH2=-267.80kJ·mol-1