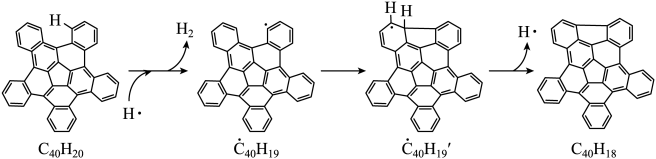
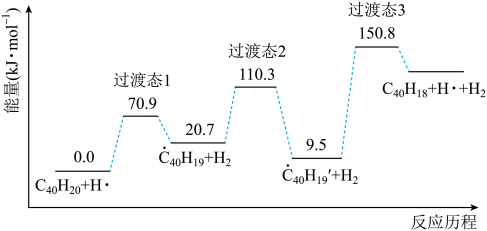
选择题
在恒温恒容密闭容器中发生反应2H2(g)+2NO(g)  2H2O(g) +N2(g),N2的瞬时生成速率v=k·cm(H2)c2 (NO)。控制NO起始浓度为0.5 mol/L,N2的瞬时生成速率和H2起始浓度的关系如图所示,下列说法正确的是( )
2H2O(g) +N2(g),N2的瞬时生成速率v=k·cm(H2)c2 (NO)。控制NO起始浓度为0.5 mol/L,N2的瞬时生成速率和H2起始浓度的关系如图所示,下列说法正确的是( )

- A、 由题可知,该反应的速率常数k为15
- B、 随着H2起始浓度增大,该反应平衡常数增大
- C、 达平衡后,H2和NO的浓度均增加一倍,则NO转化率减小
- D、 H2起始浓度0.2 mol/L,某时刻NO的浓度为0.4 mol/L,则N2的瞬时生成速率为0.24 mol/L
氨催化氧化是工业制硝酸的重要反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH<0。在T℃时,向1L密闭容器中投入4molNH3、5molO2 , 平衡时测得NH3的转化率为60%。在指定条件下,下列选项所示的物质间转化不能实现的是( )
4NO(g)+6H2O(g) ΔH<0。在T℃时,向1L密闭容器中投入4molNH3、5molO2 , 平衡时测得NH3的转化率为60%。在指定条件下,下列选项所示的物质间转化不能实现的是( )
- A、 NH3·H2O(aq)
NH4HSO4
- B、 HNO3(浓)
NO2
- C、 NH4Cl
NH3
- D、 NO
N2
精炼铜工业中阳极泥的综合利用具有重要意义,从中间产品分金渣(主要成分为: 、
、 、
、 、
、 )中获取高纯银的流程如下图所示。下列说法错误的是( )
)中获取高纯银的流程如下图所示。下列说法错误的是( )

已知:在上述反应的温度下
① ,
;
②。
- A、 “分银”时
与
反应生成
的离子方程式为
, 该反应的化学平衡常数为
- B、 “分银渣”的主要成分为
- C、 “沉银”时为防止产生污染性有毒气体,盐酸不宜过量
- D、 若“还原”时有
生成,则该反应中氧化剂与还原剂的物质的量之比为
常温下,向浓度均为0.1mol·L-1、体积均为100mL的两种一元酸HX、HY的溶液中分别加入NaOH固体,lg 随加入NaOH的物质的量的变化情况如图所示。下列叙述不正确的是( )
随加入NaOH的物质的量的变化情况如图所示。下列叙述不正确的是( )

- A、 a点由水电离出的
=1×10-13mol/L
- B、 HY溶液导电性先减弱后增强
- C、 当n(HY):n(NaY)=1:1混合配成溶液,pH=4
- D、 b点溶液中:
=
温度为T1时,在三个容积均为1L的恒容密闭容器中仅发生反应:2NO2(g) ⇌ 2NO(g)+O2(g)△H>0。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是( )
| 容器编号 | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | ||
| c(NO2) | c(NO) | c(O2) | c(O2) | |
| Ⅰ | 0.6 | 0 | 0 | 0.2 |
| Ⅱ | 0.3 | 0.5 | 0.2 | |
| Ⅲ | 0 | 0.5 | 0.35 | |
- A、 容器Ⅱ中刚开始反应时v正<v逆
- B、 达平衡时,容器I与容器Ⅱ中的总压强之比为4∶5
- C、 达平衡时,容器Ⅲ中NO的体积分数大于50%
- D、 当温度改变为T2时,若k正=k逆 , 则T2>T1
一定条件下,在容积为2 L的刚性容器中充入1 mol  (g) 和2 mol H2 , 发生反应
(g) 和2 mol H2 , 发生反应  (g)+2H2(g)
(g)+2H2(g) 
 (g) △H<0,反应过程中测得容器内压强的变化如图所示。下列说法正确的是( )
(g) △H<0,反应过程中测得容器内压强的变化如图所示。下列说法正确的是( )

- A、 升高温度可增大反应速率,提高环戊二烯的平衡转化率
- B、 0~20 min内,H2的平均反应速率为0.05 mol/(L·min)
- C、 达到平衡时,环戊烷和环戊二烯的体积分数相同
- D、 该温度下平衡常数Kp=4.0 MPa-2
温度为T时,向2.0L恒容密闭容器中充入1.0 mol PCl5 , 发生反应:PCl5(g)  PCl3(g)+Cl2(g) △H=a kJ·mol-l(a>0)。0~10 min保持容器温度不变,10 min时改变一种条件,整个过程中PCl5、PCl3、Cl2的物质的量随时间的变化如图所示。下列说法正确的是( )
PCl3(g)+Cl2(g) △H=a kJ·mol-l(a>0)。0~10 min保持容器温度不变,10 min时改变一种条件,整个过程中PCl5、PCl3、Cl2的物质的量随时间的变化如图所示。下列说法正确的是( )
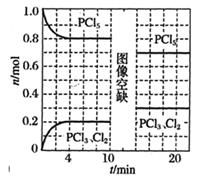
- A、 0~4 min的平均速率v(PCl3)=0.025 mol·L-1·min-1
- B、 10 min时改变的条件是增加了一定量的PCl5
- C、 若起始时向该容器中充入2.0mol PCl3和2.0 mol Cl2 , 保持温度为T, 反应达平衡时放出的热量小于1.6akJ
- D、 温度为T,起始时向该容器中充入1.0mol PCl5、0.10mol PCl3和0.10 mol Cl2 , 反应达到平衡前v正<v逆
相同温度下,甲、乙两个恒容密闭容器均进行反应:X(g)+Y(g)  W(?)+2Z(g)△H<0.实验过程中部分数据如表所示。
W(?)+2Z(g)△H<0.实验过程中部分数据如表所示。
| 容器 | 起始容积 | 物质的起始加入量 | 平衡时Z的物质的量浓度 |
| 甲 | 2L | 1molX、1molY | 0.6mol·L-1 |
| 乙 | 5L | 2molW、4molZ | 0.48mol·L-1 |
下列说法错误的是( )
- A、 该温度下W为非气态
- B、 适当降低乙容器的温度可能使c甲(Z)=1.5c乙(Z)
- C、 该温度下反应的化学平衡常数K=9
- D、 平衡后正反应速率v正(X):甲>乙
温度  ℃,反应
℃,反应  中所有物质均为气态。在起始温度、体积相同(
中所有物质均为气态。在起始温度、体积相同(  ℃、2L密闭容器)时,发生反应的部分数据见下表:
℃、2L密闭容器)时,发生反应的部分数据见下表:
| 反应条件 | 反应时间 | | | | |
| 反应Ⅰ: 恒温恒容 | 0 | 2 | 6 | 0 | 0 |
| 10 | 4.5 | ||||
| 20 | 1 | ||||
| 30 | 1 | ||||
| 反应Ⅱ: 绝热恒容 | 0 | 0 | 0 | 2 | 2 |
下列说法正确的是( )
- A、 对反应I,前10
内的平均反应速率
- B、 在其他条件不变的情况下,若30
时只向容器中再充入1
和1
,则平衡正向移动
- C、 对于反应I,进行30
时,
所占的体积分数为30%
- D、 达到平衡时,反应I、II对比:平衡常数
在体积恒为1L的密闭容器中发生反应:  。测得不同条件下A的平衡转化率a(A)如下表。
。测得不同条件下A的平衡转化率a(A)如下表。
| 实验序号 | 实验温度 | 初始投料量 | | |
| | | |||
| 1 | | 10 | 10 | 50 |
| 2 | | 10 | 10 | a |
| 3 | | 15 | 10 | 40 |
下列说法正确的是( )
- A、 当容器内压强不变时,反应达到化学平衡状态
- B、
时,反应的化学平衡常数值为2
- C、 若
,则
- D、
某温度下,H2(g)+CO2(g)  H2O(g)+CO(g)的平衡常数K=
H2O(g)+CO(g)的平衡常数K=  。该温度下,在①、②两个恒容密闭容器中投入H2(g)和CO2(g),起始浓度如下表。下列说法正确的是( )
。该温度下,在①、②两个恒容密闭容器中投入H2(g)和CO2(g),起始浓度如下表。下列说法正确的是( )
| 容器编号 | 起始浓度/mol·L−1 | |||
| H2 | CO2 | H2O | CO | |
| ① | 0.1 | 0.1 | 0 | 0 |
| ② | 0.2 | 0.1 | 0.2 | 0.1 |
- A、 反应开始时,②中反应向逆反应方向进行
- B、 平衡时,①中c(CO2)=0.04mol·L−1
- C、 ①中H2的平衡转化率为40%
- D、 ①、②均达平衡时,①中各组分浓度与②相同
工业上可用“丙烯氨氧化法”生产重要的化工原料丙烯腈(C3H3N)。
①在催化剂存在下生成丙烯腈(C3H3N)的热化学方程式为C3H6(g)+NH3(g)+3/2O2(g)=C3H3N(g)+3H2O(g) ΔH=-515 kJ/mol
②得到副产物丙烯醛(C3H4O)的热化学方程式为C3H6(g)+O2(g)=C3H4O(g)+H2O(g) ΔH=-353kJ/mol
丙烯腈产率与反应温度的关系曲线如图所示。
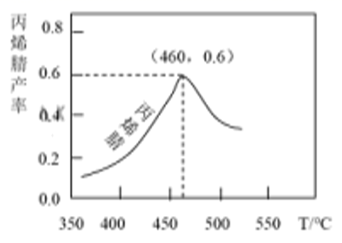
下列说法错误的是( )
- A、 反应①的平衡常数可表示为K=
- B、 增大压强可以提高丙烯腈的平衡产率
- C、 温度低于460℃时,丙烯腈的产率不是对应温度下的平衡产率
- D、 C3H4O(g)+NH3(g)+
O2(g)=C3H3N(g)+2H2O(g) ΔH=-162 kJ/mol
在一定的温度下,将一定量的氢气和氮气的混合气体充入等压密闭容器中进行反应,达到平衡时维持温度不变,测得混合气体的密度是反应前密度的1.25倍,则达到平衡时,氨气的体积分数为( )
- A、 25%
- B、 27.5 %
- C、 30%
- D、 37.5%
往恒容密闭容器中通入amolNO2气体,在一定温度下分解生成O2和NO,各物质的浓度随时间的变化如图所示。下列说法错误的是( )

- A、 X表示NO,Y表示O2
- B、 t1min时,NO2的正反应速率比逆反应速率大
- C、 t3min时,c(NO2)+c(NO)+c(O2)=1.5amol•L-1
- D、 t2min时,NO2在混合物中所占的物质的量分数为0.25