选择题
下列过程与水解反应无关的是( )
- A、 热的纯碱溶液去除油脂
- B、 重油在高温、高压和催化剂作用下转化为小分子烃
- C、 蛋白质在酶的作用下转化为氨基酸
- D、 向沸水中滴入饱和
溶液制备
胶体
一种分解氯化铵实现产物分离的物质转化关系如下,其中 代表
代表 或
或 中的一种。下列说法正确的是( )
中的一种。下列说法正确的是( )
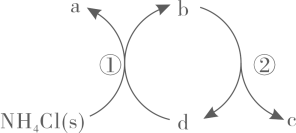

- A、
、
分别是
- B、
既可以是
, 也可以是
- C、 已知
为副产物,则通入水蒸气可减少
的产生
- D、 等压条件下,反应
、
的反应热之和,小于氯化铵直接分解的反应热
利用平衡移动原理,分析一定温度下 在不同
在不同 的
的 体系中的可能产物。
体系中的可能产物。
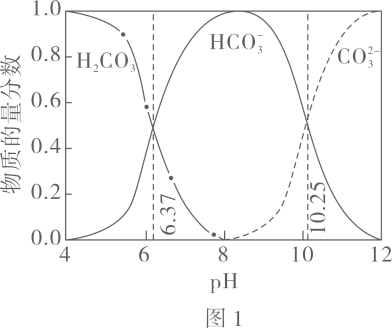
已知:图
中曲线表示
体系中各含碳粒子的物质的量分数与
的关系。
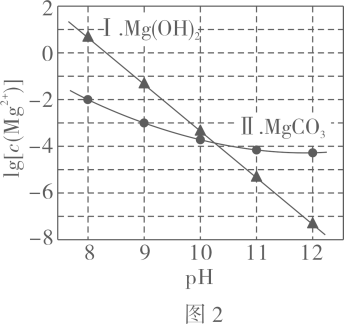
图
中曲线Ⅰ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合
注:起始
, 不同
下
由图
得到
。
下列说法不正确的是( )
- A、 由图
,
- B、 由图
, 初始状态
, 无沉淀生成
- C、 由图
, 初始状态
, 平衡后溶液中存在
- D、 由图
和图
, 初始状态
、
, 发生反应:
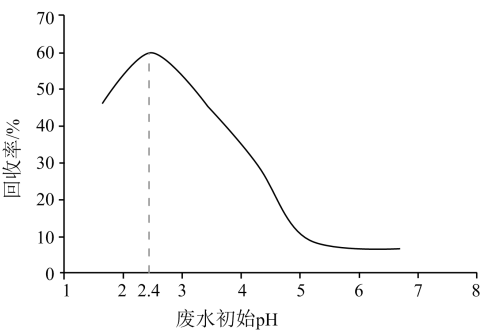
甲酸 是重要的化工原料。工业废水中的甲酸及其盐,通过离子交换树脂(含固体活性成分
是重要的化工原料。工业废水中的甲酸及其盐,通过离子交换树脂(含固体活性成分 , R为烷基)因静电作用被吸附回收,其回收率(被吸附在树脂上甲酸根的物质的量分数)与废水初始
, R为烷基)因静电作用被吸附回收,其回收率(被吸附在树脂上甲酸根的物质的量分数)与废水初始 关系如图(已知甲酸
关系如图(已知甲酸 ),下列说法错误的是
),下列说法错误的是
- A、 活性成分
在水中存在平衡:
- B、
的废水中
- C、 废水初始
, 随
下降,甲酸的电离被抑制,与
作用的
数目减少
- D、 废水初始
, 离子交换树脂活性成分主要以
形态存在
将去掉氧化膜的铝片放入足量Na2CO3溶液中,铝片表面产生气泡,充分反应后得到无色溶液M。下列分析错误的是( )
- A、 产生的气体中有H2
- B、 反应与
水解有关
- C、 Al(OH)3向酸式电离方向移动
- D、 M中含大量:Na+、Al3+、
室温下用0.1 mol∙L-1 Na2SO3溶液吸收SO2的一种脱硫工艺流程如下图所示。已知H2SO3电离平衡常数分别为Ka1=1.54×10-2 , Ka2=1.02×10-7 , H2CO3电离平衡常数分别为Ka1=4.30×10-7、Ka2=5.61×10-11 , 忽略通入SO2所引起的溶液体积变化和H2O挥发。

下列说法正确的是
- A、 0.1 mol∙L-1 Na2SO3溶液中:
- B、 NaHSO3溶液中:
- C、 “沉淀”时发生主要反应的离子方程式:
- D、 “沉淀”分离后的滤液中:
氨基酸在水溶液中可通过得到或失去 发生如下反应:
发生如下反应:

常温下,的甘氨酸(
)溶液中各微粒浓度对数值与pH的关系如图所示:

下列说法正确的是( )
- A、 曲线③为
的浓度与pH的关系图
- B、
,
- C、
平衡常数的数量级为
- D、 C点溶液中满足:
室温下,向100 mL 0.1 mol·L-1 Na2SO3(aq)中分别加(通)入不同试剂,现象见下表:
| 试剂 | 现象 | |
| 1 | 酚酞 | 溶液变红,加水稀释,红色变浅 |
| 2 | 少量SO2 | 用pH试纸测得溶液pH≈8 |
| 3 | 少量Cl2 | 无明显现象 |
下列说法错误的是( )
- A、 Na2SO3(aq)中存在:c(OH-)=c(H+)+2c(H2SO3)+c(HSO3-)
- B、 实验1中随着水的不断加入,溶液中
的值逐渐增大
- C、 实验2反应后溶液中存在:c(Na+)>c(HSO3-)+2c(SO32-)
- D、 实验3反应后溶液中存在:c(H+)=c(Cl-)
- A、
的某酸
溶液中一定存在:
- B、
的氨水溶液稀释10倍后
- C、
相同的
溶液、
溶液、
溶液,其浓度大小关系:
- D、 常温下,
溶液中,由水电离产生的
浓度为
下列物质的水溶液呈碱性且属于盐是( )
- A、 苯甲酸钠
- B、
- C、 HCl
- D、
下列“类比”不合理的是( )
- A、 丙醛能与
发生加成反应,丙酮也可以与
发生加成反应
- B、 乙烯中所有原子都在同一平面上,则2,3-二甲基-2-丁烯中所有碳也在同一平面上
- C、 往NaOH溶液通少量
, 生成
, 则往苯酚钠溶液中通入少量
, 也生成
- D、
溶液在空气中蒸干得到
固体,则
溶液在空气中蒸干也得到
固体
常温下,用0.1000 的盐酸滴定20.00mL
的盐酸滴定20.00mL  溶液,溶液中
溶液,溶液中 、
、 、
、 的分布分数
的分布分数 随pH变化曲线及滴定曲线如图。下列说法正确的是( )
随pH变化曲线及滴定曲线如图。下列说法正确的是( )

已知:
- A、
- B、
的
的值为
- C、 若将
完全转变为
, 仅需用酚酞做指示剂
- D、 图中c点,
水溶液呈酸性的盐是( )
- A、
- B、
- C、 NaH
- D、 NaClO
某二元酸(H2A)在水中的电离方程式为:H2A=H++HA- , HA- H++A2-
H++A2- , 下列说法错误的是( )
, 下列说法错误的是( )
- A、 在0.1 mol/L的Na2A溶液中,c(A2-)+c(HA-)+2c(Na+)=0.5 mol/L
- B、 25℃时,若测得0.1 mol/L的NaHA溶液pOH=a,升高温度,测得同浓度的NaHA溶液pOH=b,则b一定大于a
- C、 25℃时,将同浓度的NaHA和Na2A溶液等体积混合,其pH一定小于7
- D、 0.1 mol/L的NaHA溶液中离子浓度为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)



 )溶液中含元素X物种的浓度之和为
)溶液中含元素X物种的浓度之和为 




 已知: ① Fe(OH)3开始沉淀的 pH值为2.7,沉淀完全时的 pH值为3.7。
已知: ① Fe(OH)3开始沉淀的 pH值为2.7,沉淀完全时的 pH值为3.7。

