选择题
一定温度下,AgCl和Ag2CrO4的沉淀溶解平衡曲线如图所示。
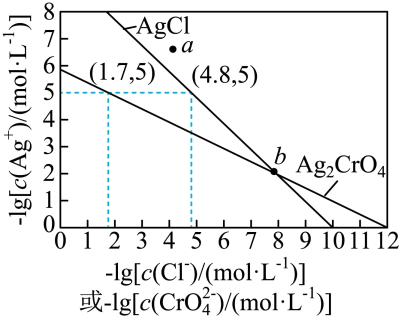
下列说法正确的是
- A、 a点条件下能生成Ag2CrO4沉淀,也能生成AgCl沉淀
- B、 b点时,c(Cl-)=c(CrO
),Ksp(AgCl)=Ksp(Ag2CrO4)
- C、 Ag2CrO4+2Cl-
2AgCl+CrO
的平衡常数K=107.9
- D、 向NaCl、Na2CrO4均为0.1mol·L-1的混合溶液中滴加AgNO3溶液,先产生Ag2CrO4沉淀
向 饱和溶液(有足量
饱和溶液(有足量 固体)中滴加氨水,发生反应
固体)中滴加氨水,发生反应 和
和 ,
,  与
与 的关系如下图所示(其中M代表
的关系如下图所示(其中M代表 、
、 、
、 或
或 )。
)。
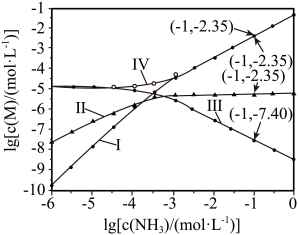
下列说法错误的是
- A、 曲线I可视为
溶解度随
浓度变化曲线
- B、
的溶度积常数
- C、 反应
的平衡常数K的值为
- D、
时,溶液中
下列说法正确的是
- A、 FeS溶于稀硫酸,而CuS不溶于稀硫酸,则
- B、 向盐酸中加入氨水至中性,溶液中
- C、 0.01
溶液:
- D、 向丙烯醛中加入溴水,溴水褪色,证明丙烯醛中含有碳碳双键
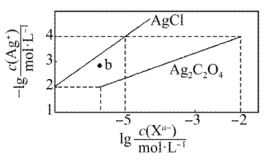
25℃时,在c(HR)+c(R-)=0.1mol·L-1的溶液中-lgc(R-)与-lgc(OH-)、难溶盐MR饱和溶液中-lgc(R-)与-lgc(M+)的关系如图所示(忽略离子浓度调节过程中溶液体积的变化)。下列说法错误的是

- A、 曲线L2表示-lgc(R-)与-lgc(OH-)的关系
- B、 25℃时,Ksp(MR)的数量级为10-20
- C、 加水稀释,两种溶液中的离子浓度不一定都减小
- D、 pH=7时,c(HR)+c(R-)=0.1mol·L-1的溶液中c(HR)<c(R-)
氯化亚铜(CuCl)是一种难溶于水的白色固体,常温下,CuCl(s) Cu+(aq)+Cl-(aq) Ksp=1.2×10-6。在氯离子浓度较大的体系中,氯化亚铜发生溶解,生成两种配合物离子:CuCl(s)+Cl-(aq)=
Cu+(aq)+Cl-(aq) Ksp=1.2×10-6。在氯离子浓度较大的体系中,氯化亚铜发生溶解,生成两种配合物离子:CuCl(s)+Cl-(aq)= (aq) K1=0.36;
(aq) K1=0.36; (aq)+Cl-(aq)
(aq)+Cl-(aq)
 (aq) K2。用盐酸溶解时,溶液中含铜粒子分布分数(δ)与c(Cl-)的关系如图所示。下列说法错误的是
(aq) K2。用盐酸溶解时,溶液中含铜粒子分布分数(δ)与c(Cl-)的关系如图所示。下列说法错误的是

- A、 常温下,反应的平衡常数K1>K2
- B、 图中交点处溶液中:c(H+)-c(OH-)>2c(Cl-)
- C、 Cu+(aq)+2Cl-(aq)
(aq)的平衡常数K=3.0×105
- D、 常温下,若溶液中几乎不含Cu+ , 则c(Cl-)至少大于0.12mol·L-1
常温下,向10mL0.10mol/LCuCl2溶液中滴加0.10mol/LNa2S溶液,滴加过程中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,已知Ksp(ZnS)>Ksp(CuS)。下列说法错误的是
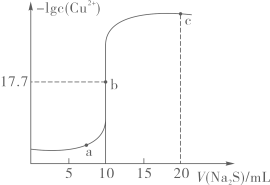
- A、 a、b两点CuS的溶度积Ksp相等
- B、 常温下,CuS的溶度积Ksp的数量级为10-36
- C、 c点溶液中:c(Cl-)>c(Na+)>c(S2-)>c(OH-)>c(H+)
- D、 闪锌矿(ZnS)遇到硫酸铜溶液可转变为铜蓝(CuS)
298K时,BaSO4与BaCO3在水中的沉淀溶解平衡曲线如图所示,下列说法错误的是

已知101.4=25
- A、 298K时,BaSO4的溶解度小于BaCO3的溶解度
- B、 U点坐标为(4,4.8)
- C、 作为分散质BaSO4 , W点v(沉淀)<v(溶解)
- D、 对于沉淀溶解平衡BaSO4(s)+CO
(aq)
BaCO3(s)+SO
(aq),其平衡常数K=0.04
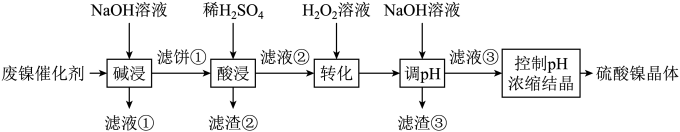
工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),其主要的生产流程如下:

已知: K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定,难溶于醇等有机溶剂。下列说法错误的是:( )
- A、 反应②为3NaClO+2Fe( NO3)3+10NaOH= 2Na2FeO4↓+3NaCl+6NaNO4+5H2O
- B、 由反应③可知,此温度下Kap(K2FeO4)>Kap(Na2FeO4)
- C、 “提纯”步骤的洗涤剂可以选用CH3COOK溶液、异丙醇
- D、 K2FeO4可用于水的消毒
常温下,分别向 浓度均为
浓度均为 的NaX溶液、
的NaX溶液、 溶液滴加
溶液滴加 溶液,pM与
溶液,pM与 溶液体积的关系如图所示[
溶液体积的关系如图所示[ ,
,  代表
代表 、
、 ],下列说法正确的是
],下列说法正确的是
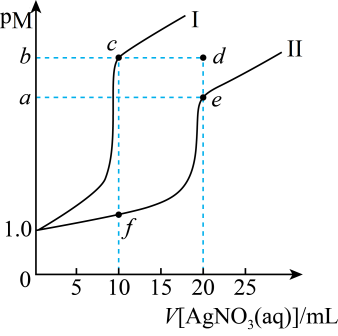
- A、 曲线Ⅱ表示
的关系图
- B、 常温下,饱和溶液的物质的量浓度:
- C、 若
变为
, 则c点向e点移动
- D、 d点是
的饱和溶液
 图标提示全部需要
图标提示全部需要