选择题
取两份 
 的
的  溶液,一份滴加
溶液,一份滴加  的盐酸,另一份滴加
的盐酸,另一份滴加  溶液,溶液的pH随加入酸(或碱)体积的变化如图。
溶液,溶液的pH随加入酸(或碱)体积的变化如图。

下列说法不正确的是( )
- A、 由a点可知:
溶液中
的水解程度大于电离程度
- B、
过程中:
逐渐减小
- C、
过程中:
- D、 令c点的
,e点的
,则
鸟嘌呤(  )是一种有机弱碱,可与盐酸反应生成盐酸盐(用
)是一种有机弱碱,可与盐酸反应生成盐酸盐(用  表示)。已知
表示)。已知  水溶液呈酸性,下列叙述正确的是( )
水溶液呈酸性,下列叙述正确的是( )
- A、
水溶液的
- B、
水溶液加水稀释,
升高
- C、
在水中的电离方程式为:
- D、
水溶液中:
常温下,用  的盐酸分别滴定20.00mL浓度均为
的盐酸分别滴定20.00mL浓度均为  三种一元弱酸的钠盐
三种一元弱酸的钠盐  溶液,滴定曲线如图所示。下列判断错误的是( )
溶液,滴定曲线如图所示。下列判断错误的是( )

- A、 该
溶液中:
- B、 三种一元弱酸的电离常数:
- C、 当
时,三种溶液中:
- D、 分别滴加20.00mL盐酸后,再将三种溶液混合:
HA是一元弱酸,难溶盐MA的饱和溶液中  而变化,
而变化,  不发生水解。实验发现,298K时
不发生水解。实验发现,298K时  ,如下图中实线所示。
,如下图中实线所示。
下列叙述错误的是( )

- A、 溶液pH = 4 时.
- B、 MA 的溶度积
- C、 溶液 pH = 7 时,
- D、 HA 的电离常数
实验测得10 mL 0.50 mol·L-1NH4Cl溶液、10 mL 0.50mol·L-1CH3COONa溶液的pH分别随温度与稀释加水量的变化如图所示。已知25 ℃时CH3COOH和NH3·H2O的电离常数均为1.8×10-5.下列说法错误的是( )
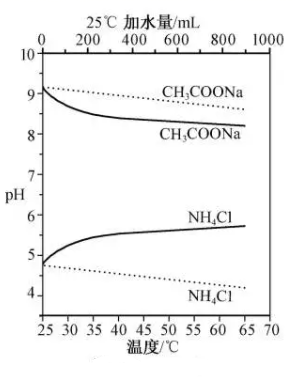
- A、 图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
- B、 将NH4Cl溶液加水稀释至浓度
mol·L-1 , 溶液pH变化值小于lgx
- C、 随温度升高,Kw增大,CH3COONa溶液中c(OH- )减小,c(H+)增大,pH减小
- D、 25 ℃时稀释相同倍数的NH4Cl溶液与CH3COONa溶液中:c(Na+ )-c(CH3COO- )=c(Cl-)-c(NH
)
常温下,向1L浓度为0.1mol/LHA溶液中逐渐加入NaOH固体的过程中,主要成分的分布分数(HA或A-占含A微粒总量的百分数)随pH的变化如图所示。忽略过程中溶液体积的变化,下列说法错误的是( )

- A、 HA的电离常数的数量级为10-5
- B、 pH=5.6时,溶液中
- C、 加入NaOH固体的质量为2.0g时,溶液的pH>7
- D、 pH=7时,溶液中c(Na+)=c(A-)
常温下,用NaOH溶液滴定二元弱酸亚磷酸溶液,溶液中- 和-lgc(
和-lgc( )或-
)或- 和-lgc(
和-lgc( )的关系如图所示,下列说法错误的是( )
)的关系如图所示,下列说法错误的是( )

- A、 L2表示-
和-lgc(
)的关系
- B、 H3PO3的电离常数Ka1(H3PO3)的数量级为10-2
- C、 等浓度等体积的H3PO3溶液与NaOH溶液充分混合,c(
)<c(H3PO3)
- D、 pH=6.54时,c(Na+ )<3c(
)
室温下,通过实验探究 溶液的性质并记录如下。下列说法错误的是( )
溶液的性质并记录如下。下列说法错误的是( )
实验 | 实验操作和现象 |
1 | 向 |
2 | 向 |
3 | 向 |
- A、 实验1证明
溶液中存在:
- B、 实验1可推测出
溶液中存在:
- C、 实验2证明氧化性:
- D、 实验3反应静置后的上层清液中存在:
常温下,用0.1 mol·L-1NaOH溶液滴定10 mL 0.1 mol·L-1H2A溶液,溶液的pH与NaOH溶液的体积关系如图所示,下列说法正确的是( )

- A、 H2A是强酸
- B、 B点:c(H2A)>c(A2- )
- C、 C点:c(Na+)<c(HA- )+ 2c(A2-)
- D、 水电离出来的c(OH- ):D点>C点>B点
柠檬酸(用 表示)是一种高效除垢剂,现用一定浓度的柠檬酸溶液去除水垢,溶液中
表示)是一种高效除垢剂,现用一定浓度的柠檬酸溶液去除水垢,溶液中 、
、 、
、 、
、 的百分含量随
的百分含量随 的变化曲线如图所示。下列说法中错误的是( )
的变化曲线如图所示。下列说法中错误的是( )

- A、
的第二步电离常数
约为
- B、
溶液中,
水解程度小于电离程度
- C、
时,
- D、
时,
水溶液中存在多种平衡,下列说法正确的是( )
- A、 稀醋酸溶液稀释时,溶液中所有离子的物质的量浓度均减小
- B、 水溶液中,pH=7时,溶液一定呈中性
- C、 物质的量浓度相等的
和
溶液等体积混合,则
- D、 用已知浓度的NaOH溶液滴定未知浓度的
溶液,若选用甲基橙做指示剂,滴定过程中水的电离程度先增大后减小
谷氨酸[ HOOC(CH2)2CH(NH2)COOH,用H2R表示]是人体内的基本氨基酸之一,在水溶液中存在如下平衡:H2R HR-
HR- R2-。常温下,向一定浓度的H2R溶液中滴加NaOH溶液,混合溶液中lgx[x表示
R2-。常温下,向一定浓度的H2R溶液中滴加NaOH溶液,混合溶液中lgx[x表示 或
或 ]随pOH[pOH=- lgc(OH- )] 的变化如图所示。下列说法正确的是( )
]随pOH[pOH=- lgc(OH- )] 的变化如图所示。下列说法正确的是( )

- A、 K1=1×10-9.7
- B、 pH=7时,c(HR-)>c(H2R)>c(R2-)
- C、 曲线II表示pOH与lg
的变化关系
- D、 M点时,c(H+ )+c(Na+ )=c(OH-)+3c(HR-)
三甲胺[N(CH3)3]是一种一元有机弱碱,可简写为MOH。常温下,向20mL0.5mol/LMOH溶液中逐滴加入浓度为0.25mol/L的HCl溶液,溶液中 ,
,  、中和率(中和率=被中和的MOH的物质的量/反应前MOH的总物质的量)的变化如图所示。下列说法错误的是( )
、中和率(中和率=被中和的MOH的物质的量/反应前MOH的总物质的量)的变化如图所示。下列说法错误的是( )

- A、 a点时,
- B、 b点时,
- C、 溶液中水的电离程度:c点>d点
- D、 三甲胺[N(CH3)3]的电离常数为
常温下,几种弱电解质的电离常数如下表所示:
下列说法正确的是( )
- A、
溶液呈中性,溶液中水的电离程度与纯水的电离程度相同
- B、
溶液中:
- C、 等浓度的
与
混合溶液中:
- D、
水溶液显碱性
室温下,向20mL浓度均为0.1 的
的 和
和 混合液中逐滴加入0.1
混合液中逐滴加入0.1 NaOH溶液,溶液pH变化曲线如图。下列说法错误的是( )
NaOH溶液,溶液pH变化曲线如图。下列说法错误的是( )

- A、 a点:
- B、 导电能力:b<c
- C、 c点:
- D、 由d点可得








