选择题
下列装置可以用于相应实验的是
| A | B | C | D |
|
|
|
|
|
| 制备 | 分离乙醇和乙酸 | 验证 | 测量 |
- A、 A
- B、 B
- C、 C
- D、 D
实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有碳等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是( )
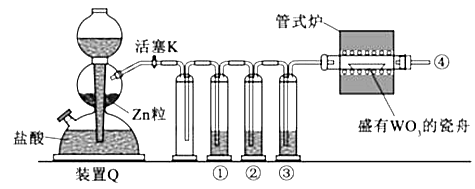
- A、 ①、②、③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液
- B、 管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体浓度
- C、 结束反应时,先关闭活塞K,再停止加热
- D、 装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
检验下列指定成分所用的试剂正确的是( )
| 选项 | 检验括号中的物质 | 检验试剂 |
| A | CO2气体(H2S) | CuSO4溶液 |
| B | Na2SO3溶液(Na2SO4) | BaCl2溶液 |
| C | 海水(KI) | 淀粉溶液 |
| D | 乙醇(水) | 金属钠 |
- A、 A
- B、 B
- C、 C
- D、 D
某同学利用下图装置来探究无水硫酸亚铁灼烧后的分解产物,实验过程中,观察到装置c中的品红溶液褪色,装置d中的溶液中有白色沉淀。下列说法错误的是( )

- A、 装置b中出现白色沉淀
- B、 加热前要先通入氮气,加热结束时也要通入氮气
- C、 实验过程中,装置a的玻璃管中固体粉末可能变红
- D、 若用足量溴水代替品红溶液,装置d中的现象不变
下列气体的验证方法没有涉及氧化还原反应的是( )
- A、 氧气——带火星的小木条复燃
- B、 氯气——湿润的有色纸条褪色
- C、 乙烯——酸性高锰酸钾溶液褪色
- D、 氨气——湿润的红色石蕊试纸变蓝
下列操作或装置,不能达到实验目的的是( )。

- A、 图Ⅰ用于实验室制氨气并收集干燥的氨气
- B、 图Ⅱ用于检验浓硫酸与铜反应后的产物中是否含有铜离子
- C、 图Ⅲ用于验证牺牲阳极的阴极保护法
- D、 图Ⅳ用于制取
晶体
化学无处不在,与化学有关的说法错误的是 ( )
- A、 侯氏制碱法的工艺过程中应用了物质溶解度的差异
- B、 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气
- C、 碘是人体必需微量元素,所以要多吃富含高碘酸的食物
- D、 黑火药由硫磺、硝石、木炭三种物质按一定比例混合制成
用下列装置完成相关实验,合理的是( )

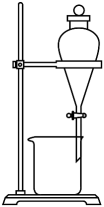
- A、 图①:验证H2CO3的酸性强于H2SiO3
- B、 图②:收集CO2或NH3
- C、 图③:分离Na2CO3溶液与CH3COOC2H5
- D、 图④:分离CH3CH2OH与CH3COOC2H5
用试纸检验气体是一种重要的实验方法.下列试纸的选用以及对应的现象、结论都正确的一项是( )
- A、 用干燥的pH试纸检验CO2
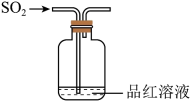
- B、 SO2能使湿润的品红试纸褪色
- C、 用干燥的红色石蕊试纸检验NH3
- D、 能使湿润的淀粉碘化钾试纸变蓝的气体一定是氯气
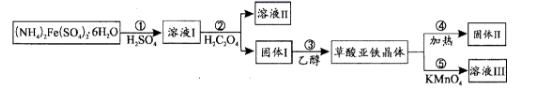
草酸亚铁晶体(FeC2O4·2H2O)是一种淡黄色粉末,某课外小组利用下列装置检验草酸亚铁晶体受热分解的部分产物。

下列说法正确的是( )
- A、 若③和⑤中分别盛放足量NaOH溶液和CuO,可检验生成的CO
- B、 实验时只需要在装置①中反应结束后再通入N2
- C、 若将④中的无水CaCl2换成无水硫酸铜可检验分解生成的水蒸气
- D、 实验结束后,①中淡黄色粉末完全变成黑色,则产物一定为铁
某同学用下图所示装置检验草酸亚铁晶体(FeC2O4·2H2O,淡黄色)受热分解的部分产物。下列说法正确的是( )

- A、 通入N2的主要目的是防止空气中的水蒸气对产物检验产生影响
- B、 若③和⑤中分别盛放足量NaOH溶液、CuO固体,可检验生成的CO
- C、 实验结束后,①中淡黄色粉末完全变成黑色,则产物一定为铁
- D、 若将④中的无水CaCl2换成无水硫酸铜可检验分解生成的水蒸气
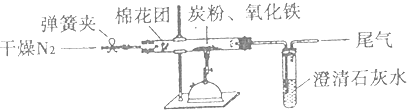
灼热的焦炭与水蒸气反应所得产物为H2、CO和少量CO2 , 为了检验产物中的H2和CO(设气体均被充分吸收),设计如下实验装置。下列有关说法错误的是( )

- A、 为了实验安全,应先点燃①处酒精灯,后点燃④处酒精灯
- B、 ②、③、⑤中依次盛装氢氧化钠溶液、浓硫酸和澄清石灰水
- C、 ④中黑色固体变红色,即可证明产物中一定含有H2和CO中的一种或两种
- D、 若用碱石灰替换无水硫酸铜,也可以达到检验H2和CO目的
下列说法正确的是( )
- A、 加热NH4Cl晶体时,将湿润的红色石蕊试纸靠近试管口,检验NH3的生成
- B、 取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+
- C、 除去KNO3中的少量NaCl,可将混合物制成热的饱和溶液,冷却结晶,过滤
- D、 通过灼热的镁粉除去N2中的O2
化学是一门以实验为基础的学科。用下列实验装置进行相应实验,能达到实验目的的是( )

- A、 图1装置可验证
的漂白性
- B、 图2装置可验证氧化性:
- C、 图3装置可制备无水
- D、 图4装置可验证氨水呈碱性
 ,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如下。
,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如下。