选择题
实验室用基准 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸滴定
配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸滴定 标准溶液。下列说法错误的是( )
标准溶液。下列说法错误的是( )
- A、 可用量筒量取
标准溶液置于锥形瓶中
- B、 应选用配带塑料塞的容量瓶配制
标准溶液
- C、 应选用烧杯而非称量纸称量
固体
- D、 达到滴定终点时溶液显橙色
- A、 恰好中和时,溶液呈碱性
- B、 滴加
溶液至
的过程中,发生反应的离子方程式为:
- C、 滴定过程中,
- D、
时,
常温下,用0.10mol·L-1的盐酸滴定20mL相同浓度的某一元碱BOH溶液,滴定过程中pH及电导率变化曲线如图所示:

下列说法错误的是( )
- A、 BOH的Kb约为1×10-5
- B、 a点:c(B+)+2c(H+)=2c(OH-)+c(BOH)
- C、 滴加盐酸的过程中,溶液中水的电离程度先减小后增大
- D、 b点:c(B+)<0.05mol·L-1
298K下,将VbmL0.1mol·L-1MOH溶液与VamL0.1mol·L-1HR溶液按Va+Vb=100混合,测得Va、Vb与混合溶液pH的关系如图所示,下列说法错误的是( )

- A、 代表Va变化的是曲线II
- B、 电离平衡常数:Kb(MOH)>Ka(HR)
- C、 pH=7的混合溶液中存在:3c(M+)+c(H+)=3c(R-)+c(OH-)
- D、 N点溶液中存在:c(HR)=c(OH-)+c(MOH)+c(H+)
常温下,向10mL 0.1mol/L的HNO2溶液中逐滴加入一定浓度的氨水,不考虑NH4NO2的分解,所得溶pH及导电能力变化如下图。下列分析正确的是( )

- A、 氨水的物质的量浓度约为0.05mol/L
- B、 b点溶液中离子浓度大小的关系: c(
)>c(
)>c(H+)>c(OH -)
- C、 a、d两点的导电能力和pH都相同
- D、 a点和b点溶液中,水的电离程度大小是a>b
MOH是一种一元弱碱,25℃时, 在20.0mL 0.1 mol·L-1MOH溶液中滴加0.1 mol·L-1盐酸V mL, 混合溶液的pH与 的关系如图所示。下列说法错误的是( )
的关系如图所示。下列说法错误的是( )

- A、 x=3.75
- B、 a点时,V=10.0 mL
- C、 25℃时, MOH的电离常数Kb的数量级为10-4
- D、 V=20.0 mL时,溶液存在关系: 2c(H+) + c(M+) = c(MOH) +2c(OH-)+ c(Cl-)
25℃时,用0.100 mol·L -1NaOH溶液滴定0.100 mol·L-1顺丁烯二酸H2A溶液,溶液中主要粒子的分布系数 (例如
(例如 图中实线)以及pH(图中虚线)随V(NaOH溶液)变化如图。下列叙述错误的是( )
图中实线)以及pH(图中虚线)随V(NaOH溶液)变化如图。下列叙述错误的是( )

- A、
对应的粒子为HA-
- B、 NaHA溶液中c(Na+)>c(HA- )> c(H2A)>c(A2-)
- C、 H2A的电离常数
- D、 顺丁烯二酸H2A溶液体积为25.0 mL
用0.10 的NaOH溶液分别滴定20.00mL浓度为c1的醋酸、c2的草酸(H2C2O4)溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点。下列说法错误的是( )
的NaOH溶液分别滴定20.00mL浓度为c1的醋酸、c2的草酸(H2C2O4)溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点。下列说法错误的是( )

- A、 由滴定曲线可判断:c1>c2
- B、 滴定过程中始终有n(CH3COOH)=0.02c1+n(OH-)-n(H+)-n(Na+)
- C、 若a点V(NaOH)=7.95 mL,则a点有c(Na+)>c(C2O
)>c(HC2O
)>c(H2C2O4)
- D、 若b点时溶液中c(CHCOO-)=c(CHCOOH),则b点消耗了8.60mL的NaOH溶液
用已知浓度盐酸滴定未知浓度 溶液,甲基橙作指示剂。若测定结果偏低,可能原因是( )
溶液,甲基橙作指示剂。若测定结果偏低,可能原因是( )
- A、 滴定管用蒸馏水洗净后未用盐酸润洗
- B、 盛装待测液的锥形瓶水洗后未烘干
- C、 滴定过程中振荡锥形瓶时不慎有少量液体溅出
- D、 滴定至锥形瓶中溶液颜色由橙变红,且
内不改变时停止

- A、 当
时,混合溶液pH≈4.2
- B、 滴入10mLKOH溶液时,溶液呈酸性
- C、 滴入20mLKOH溶液时,溶液中
- D、 滴入KOH溶液的过程中,可能出现
常温下,用0.1mol/L盐酸滴定25.00mL 0.1mol/L弱碱MOH溶液,溶液中pH、分布系数δ随滴加盐酸体积[V(盐酸)]的变化关系如图所示。[如δ(M+)=  ]。 下列叙述错误的是( )
]。 下列叙述错误的是( )

下列叙述错误的是
- A、 曲线①代表δ(M+),曲线③代表δ(MOH)
- B、
= 1.0 ×10-5.1
- C、 点a溶液中c(M+)+c(MOH)> 2c(Cl-)
- D、 图中V1> 12.5mL
室温下,向20.00mL0.1000mol/L的某一元碱MOH溶液中滴加未知浓度的稀硫酸,混合溶液的温度、酸度AG[AG=  随加入稀硫酸体积的变化如图所示。下列说法正确的是( )
随加入稀硫酸体积的变化如图所示。下列说法正确的是( )

- A、 硫酸的浓度为0.1000mol/L
- B、 b点对应的溶液中:c(M+)+2c(H+)=2c(OH-)+c(MOH)
- C、 当AG=0时,溶液中存在:c(
)>c(M+)>c(H+)=c(OH-)
- D、 b、c、d三点对应的溶液中,水的电离程度的大小关系是b>c>d
已知H3R是一种三元中强酸。25℃时,向某浓度H3R溶液中逐滴加入NaOH溶液(保持温度不变),各种含R微粒的物质的量分数δ随溶液pH的变化曲线及交点的pH如图所示。下列说法正确的是( )

- A、 pH=7.15时,c(H2R-)>c(HR2-)
- B、 随着NaOH溶液的加入,c(R3-)逐渐增大,水的电离程度逐渐增大
- C、 25℃时,HR2-的水解平衡常数为Kh2 , 则
- D、 滴加过程中c(H3R)+c(H2R-)+c(HR2-)+c(R3-)保持不变
常温下,向某浓度的  溶液中逐滴加入NaOH溶液,溶液中-lgc(x)(x为H2A、HA-或A2-)与溶液pH的变化关系如图所示。则下列说法正确的是( )
溶液中逐滴加入NaOH溶液,溶液中-lgc(x)(x为H2A、HA-或A2-)与溶液pH的变化关系如图所示。则下列说法正确的是( )
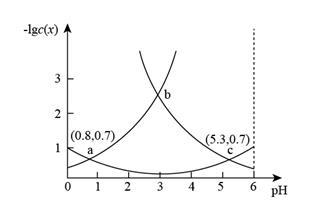
- A、 c点溶液中c(Na+)>3c(A2-)
- B、 整个过程中[c(H2A)+c(HA-)+c(A2-)]保持不变
- C、 将等物质的量浓度的NaHA与H2A溶液等体积混合,所得溶液pH=0.8
- D、 b点对应溶液的pH为3.05
常温下,向20mL0.2mol/LH2X溶液中滴加0.2mol/LNaOH溶液,溶液中各微粒的物质的量分数随pH的变化如图所示,以下说法错误的是( )

- A、 由图可推测,H2X为弱酸
- B、 滴加过程中发生的反应有:H2X+OH-=HX-+H2O,HX-+OH-=X2-+H2O
- C、 水的电离程度:a点与b点大致相等
- D、 若常温下Ka(HY)=1.1×10-2 , HY与少量Na2X发生的反应是:2HY+X2-=H2X+2Y-
常温下,二元弱酸H2Y溶液中滴加KOH溶液,所得混合溶液的pH与离子浓度变化的关系如图所示,下列有关说法错误的是

- A、 曲线M表示pH与lg
的变化关系
- B、 NaHY溶液显酸性
- C、 交点d对应的pH=2.8
- D、 e点溶液中:c(HY-)>c(H2Y)>c(Y2-)>c(H+)>c(OH-)












