选择题
已知 的速率方程为
的速率方程为 。
。 , 为探究反应速率与
, 为探究反应速率与 的关系,进行如下实验:向锥形瓶中加入一定体积(V)的2.0 mol⋅L
的关系,进行如下实验:向锥形瓶中加入一定体积(V)的2.0 mol⋅L 
 溶液、2.0 mol⋅L
溶液、2.0 mol⋅L
 溶液、1.0 mol⋅L
溶液、1.0 mol⋅L 醋酸和水,充分搅拌,保持体系温度为36℃,用秒表测量收集1.0 mL
醋酸和水,充分搅拌,保持体系温度为36℃,用秒表测量收集1.0 mL  所需要的时间(t),实验数据如下表。下列说法正确的是
所需要的时间(t),实验数据如下表。下列说法正确的是
实验 | V/mL | t/s | |||
|
| 醋酸 | 水 | ||
1 | 4.0 | 4.0 | 8.0 | 332 | |
2 | 6.0 | 4.0 | 4.0 | 6.0 | 148 |
3 | 4.0 | 4.0 | 4.0 | 83 | |
4 | 12.0 | 4.0 | 4.0 | 37 | |
- A、
;
- B、 实验3用
表示的反应平均速率
mol·s
- C、 醋酸不参与反应,其浓度的大小对该反应速率无影响
- D、 速率方程中
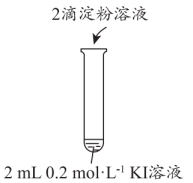
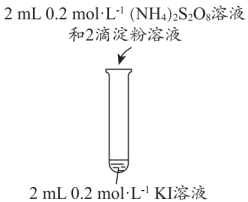
探究影响H2O2分解速率的影响因素,实验方案如图。

下列说法错误的是
- A、 对比①②,可探究FeCl3溶液对H2O2分解速率的影响
- B、 对比②③④,可探究温度对H2O2分解速率的影响
- C、 H2O2是直线形的非极性分子
- D、 H2O2易溶于水,主要是由于H2O2与H2O分子之间能形成氢键
下列实验方案(图中部分夹持略),不能达到实验目的的是
选项 | A | B | C | D |
目的 | 制取无水 | 检验产生的 | 证明 | 探究化学反应速率的影响因素 |
实验方案 |
|
|
|
|
- A、 A
- B、 B
- C、 C
- D、 D
某同学对甲苯与高锰酸钾水溶液反应速率做了如下两个实验探究:
实验I.取一定量的甲苯与一定体积和一定浓度的高锰酸钾水溶液,混合,振荡10min,缓慢褪色。
实验Ⅱ.在实验I的试剂取量基础上,再加入120g/L的冠醚(18-冠-6),振荡,4.5min褪色。
下列有关说法错误的是
- A、 实验I反应速率小的原因是高锰酸钾不溶于甲苯,氧化剂MnO
与还原剂甲苯接触不充分
- B、 K+与冠醚形成超分子,这种超分子可溶于甲苯
- C、 冠醚依靠其与K+之间的弱配位键作用,实现对K+的识别
- D、 冠醚可用作相转移催化剂
实验探究H2O2分解速率影响因素。H2O2浓度在不同条件下随时间变化的曲线如图所示。实验分组及反应条件分别为:

分组 | 温度/℃ | pH | c(Mn2+)/mol·L-1 |
① | 60 | ≈7 | 0.00002 |
② | 60 | 12 | 0 |
③ | 60 | 13 | 0 |
④ | 60 | 11 | 0.00002 |
⑤ | 70 | 13 | 0 |
下列说法不正确的是( )
- A、 实验①、④说明中性条件下,少量Mn2+对H2O2分解的影响不大
- B、 实验②、③说明其他条件相同时,溶液碱性越强,H2O2分解速率越大
- C、 实验③、⑤说明温度升高可以增大H2O2分解速率
- D、 实验④反应到40min时的化学反应速率为0.0225mol·L-1·min-1
某小组同学设计实验探究镁与铵盐溶液的反应,记录如下:
| 实验编号 | ① | ② | ③ | ④ |
| 溶液种类 | 1 | 0.5 | 0.1 | |
| | 0.48 | 0.48 | 0.48 | 0.48 |
| V(溶液) | 100 | 100 | 100 | 100 |
| 实验现象 | 有气体产生,并产生白色沉淀 | 有气体产生,并产生白色沉淀 | 有气体产生,并产生白色沉淀 | 几乎看不到现象 |
| 6h时 | 433 | 255 | 347 | 12 |
根据上述实验所得结论正确的是( )
- A、 实验②中发生的反应为
- B、 由实验①、③可得,溶液中
越大,反应速率越快
- C、 由实验①、②可得,溶液中阴离子的种类对产生
的速率有影响
- D、 由实验①~④可得,溶液的
越小,产生
的速率越快
下列实验方案不能达到相应目的的是( )
| A | B | C | ||
| 目的 | 研究浓度对化学平衡的影响 | 研究反应物之间的接触面积对化学反应速率的影响 | 制备氢氧化铁胶体 | 实验室制备并收集乙酸乙酯 |
| 实验方案 | | | | |
- A、 A
- B、 B
- C、 C
- D、 D
某小组同学探究SO2与Fe3+盐溶液的反应,进行了如下实验:已知:Fe3++HSO3-⇌Fe(HSO3)2+(红棕色)

结合上述实验,下列说法错误的是( )
- A、 产生红棕色物质的反应速率快于SO2与Fe3+氧化还原反应的速率
- B、 ①与②对照,说明阴离子种类对SO2与Fe3+氧化还原反应的速率有影响
- C、 Fe(NO3)3溶液中加入1滴浓硝酸后变为无色,说明浓硝酸具有漂白性
- D、 5h后③比①黄色更深不能证明是NO3-浓度的增大减慢了SO2与Fe3+反应的速率