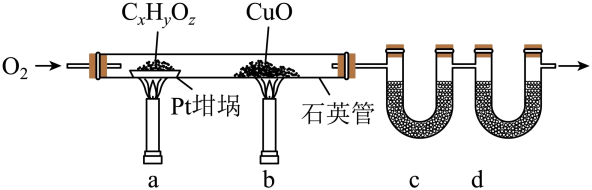
选择题
利用如图所示装置(夹持装置略)进行实验,b中现象不能证明a中产物生成的是( )
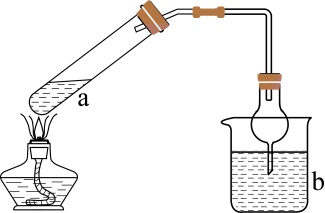
a中反应 | b中检测试剂及现象 | |
A | 浓 | 淀粉 |
B |
| 品红溶液褪色 |
C | 浓 | 酚酞溶液变红 |
D |
| 溴水褪色 |
- A、 A
- B、 B
- C、 C
- D、 D
依据下列实验,预测的实验现象正确的是( )
选项 | 实验内容 | 预测的实验现象 |
A |
| 产生白色沉淀后沉淀消失 |
B |
| 溶液变血红色 |
C | AgI悬浊液中滴加NaCl溶液至过量 | 黄色沉淀全部转化为白色沉淀 |
D | 酸性 | 溶液紫红色褪去 |
- A、 A
- B、 B
- C、 C
- D、 D
某同学为测定某NaHCO3(含少量NaCl)固体中NaHCO3的含量,设计如下实验。

下列说法错误的是
- A、 NaHCO3的质量分数为:
- B、 可通过恒重操作确保固体完全烘干
- C、 反应的离子方程式为:HCO
+Ba2++OH-=BaCO3↓+H2O
- D、 确定Ba(OH)2是否过量的操作:取上层清液,继续加Ba(OH)2溶液,看有无沉淀生成
实验室模拟吸收 , 将
, 将 按相同的流速通入不同的吸收液,当吸收液达饱和时,停止通
按相同的流速通入不同的吸收液,当吸收液达饱和时,停止通 , 记录吸收
, 记录吸收 的时间,检测部分微粒的物质的量浓度和吸收液上方有害气体残留,实现数据如下表。下列说法错误的是
的时间,检测部分微粒的物质的量浓度和吸收液上方有害气体残留,实现数据如下表。下列说法错误的是
编号 | 吸收液类型(体积相同) | c/(mol/L) | 吸收氯气时间 | 饱和吸收后溶液微粒浓度 | 液面上有害气体 | |||
pH | ||||||||
Ⅰ | 1.2 | 18′34″ | 0.56 | 未检出 | 1.81 | 1.4 | ||
Ⅱ | NaOH | 2.4 | 23′17″ | 未检出 | 0.10 | 3.23 | 5.2 | |
Ⅲ | 1.2+2.4 | 23′47″ | 未检出 | 未检出 | 3.47 | 3.4 | 无 | |
说明:表示溶液中+4价含硫微粒的总浓度,其他类似。
- A、
溶液显碱性
- B、 实验Ⅰ吸收过程中发生了氧化还原反应和复分解反应
- C、 实验Ⅱ吸收过程中生成的+1价Cl会转变为
- D、 实验Ⅲ吸收过程中NaOH与
分别与
独立反应、互不影响
《神农本草经》记载:“神农尝百草,日遇七十二毒,得茶而解。”茶叶中铁元素的检验可经以下四个步骤完成,各步骤中选用的实验用品不能都用到的是( )

- A、 将茶叶灼烧灰化,选用①、②和⑨
- B、 用浓盐酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦
- C、 过滤得到滤液,选用④、⑤和⑦
- D、 检验滤液中的Fe3+ , 选用③、⑧和⑩
以镀镍行业产生的含铁、铜、锌等杂质的酸性硫酸镍废液为原料获得NiSO4·6H2O,其工艺流程如下:(已知:Ksp[Ni(OH)2]=2.0×10-15、Ksp[Cu(OH)2]=4.8×10-20 , Ksp[Zn(OH)2]=2. 09×10-20)。下列说法错误的是( )

- A、 用KSCN溶液可以检验滤液中Fe3+是否除干净
- B、 萃取的目的是除去Cu2+和Zn2+ , 反萃取获得的有机物可循环使用
- C、 萃取振荡时分液漏斗的下口应倾斜向上
- D、 操作II的名称为蒸发结晶、过滤、洗涤干燥
某小组探究Cu与H2O2在不同条件下的反应,实验结果如表:
| 装置 | 实验 | 试剂a | 现象与结果 |
| | I | 10h后,液体变为浅蓝色,将铜片取出、干燥,铜表面附着蓝色固体,成分是Cu(OH)2 | |
| II | 8mL5mol/L氨水 | 立即产生大量气泡,溶液变为深蓝色,将铜片取出、干燥,铜表面附着蓝色固体,成分是Cu(OH)2 | |
| III | 8mL5mol/L氨水和1gNH4Cl固体 | 立即产生大量气泡,溶液变为深蓝色,将铜片取出、干燥,铜片依然保持光亮 |
下列说法错误的是( )
- A、 I中生成Cu(OH)2的反应是Cu+H2O2=Cu(OH)2
- B、 由实验可知,增大c(OH-),H2O2的氧化性增强
- C、 增大c(NH4+)有利于[Cu(NH3)4]2+的生成
- D、 [Cu(NH3)4]2+可能是H2O2分解的催化剂
检验下列溶液是否变质,所选试剂合理的是( )
| 选项 | A | B | C | D |
| 溶液 | Na2SO3溶液. | FeSO4溶液 | KI溶液 | NaOH溶液 |
| 所选试剂 | BaCl2溶液 | KSCN溶液 | AgNO3溶液 | 高锰酸钾溶液 |
- A、 A
- B、 B
- C、 C
- D、 D
将 的
的 溶液和
溶液和 溶液等体积混合,取混合液分别完成下列实验:
溶液等体积混合,取混合液分别完成下列实验:
实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
③ | 滴入 | 有蓝色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
下列说法错误的是( )
- A、 由实验①和②不能说明
与
没有发生反应
- B、 由实验③和④说明
与
发生反应
- C、 由实验①和③说明
与
发生的是可逆反应
- D、 由实验②和④说明
与
发生的是可逆反应
无色溶液中可能含有Na+、K+、 、Ca2+、Cu2+、
、Ca2+、Cu2+、 、
、 、Cl-、Br-、
、Cl-、Br-、 中的若干种,离子的物质的量浓度都为0.1 mol/L。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如图所示实验,则下列关于原溶液的判断正确的是( )
中的若干种,离子的物质的量浓度都为0.1 mol/L。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如图所示实验,则下列关于原溶液的判断正确的是( )

- A、 无法确定原溶液中是否存在Cl-
- B、 肯定存在的离子是
、Br- , 是否存在Na+、K+需要通过焰色反应来确定
- C、 肯定不存在的离子是Ca2+、Cu2+、
、
, 是否含
另需实验验证
- D、 若步骤中Ba(NO3)2和HNO3的混合溶液改用BaCl2和盐酸的混合溶液,则对溶液中离子的判断无影响
某白色固体混合物由NaOH、K2CO3、BaCl2、KAl(SO4)2∙12H2O中的两种物质组成,进行如下实验:①混合物溶于水,得到澄清透明溶液;②做焰色反应,通过钴玻璃可观察到紫色;③向溶液中加少量盐酸,产生白色沉淀。根据实验现象可判断其组成为( )
- A、 NaOH、K2CO3
- B、 NaOH、KAl(SO4)2∙12H2O
- C、 K2CO3、BaCl2
- D、 BaCl2、KAl(SO4)2∙12H2O
某固体混合物中可能含有:K+、  、Al3+、 Br-、
、Al3+、 Br-、  、
、  、
、  等离子,某同学为了确认其成分进行了实验探究,实验及现象如下(所加试剂均足量):
等离子,某同学为了确认其成分进行了实验探究,实验及现象如下(所加试剂均足量):

下列说法正确的是( )
- A、 气体A中可能含有SO2
- B、 固体混合物中一定含有Br-、
和
- C、 固体混合物中一定不含Al3+
- D、 为确定固体混合物中是否含K+ , 需进行焰色反应实验
过氧化钠可作呼吸面具中的供氧剂,实验室可用下图装置制取少量过氧化钠。下列说法错误的是( )

- A、 装置X 还可以制取H2、CO2 等气体
- B、 ②中所盛试剂为饱和小苏打溶液
- C、 ③的作用是防止空气中的水蒸气和二氧化碳进入直通玻璃管
- D、 实验时需先让 X 装置反应一会儿,再点燃装置Z中的酒精灯