单选题(1-10题,每小题2分,11-16题,每小题4分,共44分)
化学与社会、科学、技术、环境密切相关,下列说法错误的是( )
- A、 医用硝酸铵速冷冰袋是利用硝酸铵溶于水吸热的性质
- B、 夏天面粉的发酵速率与冬天面粉的发酵速率相同
- C、 合理利用太阳能、风能和氢能等能源有利于实现“低碳经济”
- D、 铁触媒的使用有利于提高合成氨的生产效率
下列各组物质中,都是弱电解质的是( )
- A、 盐酸、
、
- B、 HClO、
、
- C、 NaOH、
、
- D、
、
、
已知:X(g)+2Y(g)  3Z(g) △H= - akJ·mol-1 (a>0),下列说法不正确的是( )
3Z(g) △H= - akJ·mol-1 (a>0),下列说法不正确的是( )
- A、 0.1molX和0.2molY充分反应生成Z的物质的量一定小于0.3mol
- B、 达到化学平衡状态时,X、Y、Z的浓度不再发生变化
- C、 密闭容器中,恒温,缩小体积,X的转化率不变
- D、 升高反应温度,逆反应速率增大,正反应速率减小
室温下,对于1L 0.1mol·L-1醋酸溶液,下列判断正确的是( )
- A、 该溶液中CH3COO- 的粒子数为6.02×1022
- B、 适当升高溶液温度,溶液中导电粒子数目减小
- C、 滴加NaOH溶液过程中,n(CH3COO-)与n(CH3COOH)之和始终为0.1 mol
- D、 若该醋酸溶液的电离度为1%,则该醋酸溶液的电离平衡常数为10-4
铅蓄电池的两极分别为Pb、PbO2 , 电解质溶液为H2SO4溶液,工作时的电池反应为:
Pb+ PbO2+2H2SO4 =2PbSO4+2H2O,下列结论正确的是( )
- A、 Pb为正极,被氧化
- B、 电池工作时,电解质溶液的pH不断减小
- C、
向PbO2极移动
- D、 电池工作时,电解质溶液的pH不断增大
常温下,下列各组离子在指定溶液中因完全双水解而不能大量共存的是( )
- A、 pH=1的溶液中:Fe2+、
、
、Na+
- B、 H+、NH4+、CH3COO-、
- C、 由水电离的c(H+)=1×10-14 mol/L的溶液中:Ca2+、K+、Cl-、
- D、 K+、Al3+、
、AlO2-
已知下列3个热化学方程式(K为平衡常数):
①
②
③
则ΔH3和K3的表达式分别为( )
- A、
,
- B、
,
- C、
,
- D、
,
广义的水解观认为:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别离解成两部分,然后两两重新组合成新的物质。根据上述观点,下列说法不正确的是( )
- A、 BaO2的水解产物是Ba(OH)2和H2O2
- B、 PCl3的水解产物是HClO和H3PO4
- C、 Al4C3的水解产物是Al(OH)3和CH4
- D、 CH3COCl的水解产物是两种酸
常温下0.1 mol·L-1 ①CH3COOH、②NaOH、③CH3COONa,下列叙述正确的是( )
- A、 ①中c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
- B、 ①②等体积混合后,醋酸根离子浓度小于③的二分之一
- C、 ①③等体积混合以后,溶液呈酸性,则c(Na+)>c(CH3COO-)>c(H+)
- D、 ①②等体积混合以后,水的电离程度比①③等体积混合后水的电离程度小
某温度下向含AgCl固体的AgCl饱和溶液中加少量稀盐酸,下列说法正确的是( )
- A、 AgCl的溶解度、Ksp均减小
- B、 AgCl的溶解度、Ksp均不变
- C、 AgCl的溶解度减小、Ksp不变
- D、 AgCl的溶解度不变、Ksp减小
在密闭容器中进行反应:X(g)+3Y(g) ⇌2Z(g),有关下列图像的说法错误的是( )
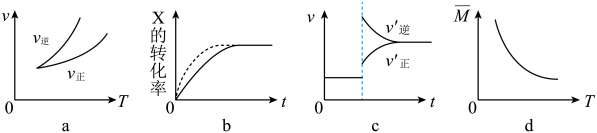
- A、 依据图a可判断正反应为放热反应
- B、 在图b中,虚线可表示使用了催化剂
- C、 若正反应的△H>0,图c可表示升高温度正逆化学反应v-t图
- D、 由图d中混合气体的平均相对分子质量随温度的变化情况,可知正反应ΔH<0
部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离平衡常数(25℃) | Ka1=1.77×10-4 | Ka1=4.9×10-10 | Ka1=4.3×10-7 ; Ka2=5.6×10-11 |
下列选项错误的是( )
- A、 向NaCN溶液中通入少量CO2气体:CN-+H2O+CO2=HCN+HCO
- B、 相同浓度的HCN和NaHCO3的导电能力:HCN>NaHCO3
- C、 中和等体积、等pH的HCOOH和HCN消耗NaOH的量,前者小于后者
- D、 等pH的HCOOH和HCN稀释相同的倍数后,pH前者大于后者
下列关于中和滴定的说法正确的是( )
- A、 用标准浓度HCl溶液滴定弱碱MOH溶液来测定其浓度,选择酚酞为指示剂
- B、 除去碱式滴定管胶管内气泡的方法是将尖嘴垂直向下,挤压胶管内的玻璃球将气泡排出
- C、 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
- D、 用稀NaOH滴定盐酸,用酚酞作指示剂,当锥形瓶中溶液由红色变无色时立即停止滴定
实验测得0.5 mol·L-1CH3COONa溶液、0.5 mol·L-1CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是( )
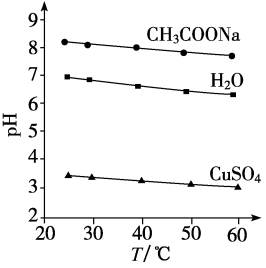
- A、 随温度升高,纯水中c(H+)>c(OH-)
- B、 随温度升高,CH3COONa溶液的pH降低,是因为CH3COO-水解平衡向逆反应方向移动
- C、 随温度升高,CH3COONa溶液的c(OH-)减小
- D、 随温度升高,CuSO4溶液的pH减小是水的电离平衡和水解平衡向正反应方向移动的结果
采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇(CH3OH)方向取得重要进展,该反应历程如图所示。下列说法错误的是( )
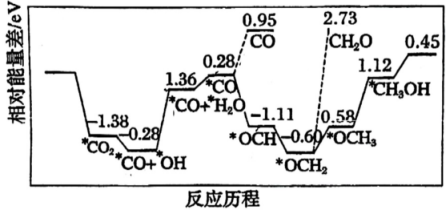
- A、 总反应焓变
- B、 上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低*CO+*OH→*CO+*H2O的能量
变化。
- C、 该催化剂可有效提高反应物的平衡转化率
- D、 容易得到的副产物有CO和CH2O,其中相对较多的副产物为CO