试题详情
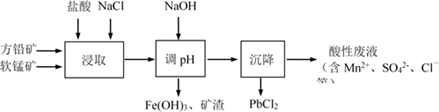
PbCl2是一种重要的化工材料,常用作助溶剂、制备铅黄等染料。工业生产中利用方铅矿精矿(主要成分为PbS,含有FeS2等杂质)和软锰矿(主要成分为MnO2)制备PbCl2的工艺流程如下图所示。
已知:i. PbCl2微溶于水
ii. PbCl2 (s) + 2Cl-(aq) PbCl42-(aq) ΔH> 0
下列说法不正确的是( )
- A、浸取过程中MnO2与PbS发生反应的离子方程式为:8H++2Cl-+PbS + 4MnO2 = PbCl2 +4Mn2++SO42-+4H2O
- B、PbCl2微溶于水,浸取剂中加入饱和NaCl溶液会增大其溶解性
- C、调pH的目的是除去Fe3+ , 因此pH越大越好
- D、沉降池中获得PbCl2采取的措施有加水稀释、降温
知识点

参考答案