试题详情
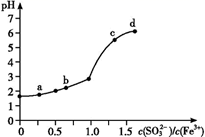
向FeCl3溶液中加入Na2SO3溶液,测定混合后溶液pH随混合前溶液中  变化的曲线如图所示。
变化的曲线如图所示。
实验发现:
ⅰ.a 点溶液澄清透明,向其中滴加 NaOH 溶液后,立即产生灰白色沉淀,滴入 KSCN 溶液显红色;
ⅱ.c 点和 d 点溶液中产生红褐色沉淀,无气体逸出;取其上层清液滴加NaOH溶液后无明显现象,滴加 KSCN 溶液显红色。
下列分析合理的是( )
- A、检验a点溶液中反应生成的阴离子所需试剂为:稀硝酸和BaCl2溶液
- B、c点和d点出现上述现象的主要原因是Fe3+和
发生双水解反应
- C、b点较a点溶液pH升高的主要原因:2Fe3++
+H2O = 2Fe2++
+2H+
- D、向d点上层清液中滴加 NaOH溶液无明显现象,证明溶液中无Fe3+
知识点

参考答案