试题详情
人们曾认为 

 的化学反应速率小,原材料利用率低,不可能用于工业化生产。化学家们不断地研究和改进该反应的条件,如催化剂、温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。从此,人类能为植物的生长提供足够的氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
的化学反应速率小,原材料利用率低,不可能用于工业化生产。化学家们不断地研究和改进该反应的条件,如催化剂、温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。从此,人类能为植物的生长提供足够的氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
合成氨是人类科学技术上的一项重大突破,曾三次获诺贝尔化学奖:
1918年弗里茨·哈伯因发明用氮气和氢气合成氨的方法获得诺贝尔化学奖,
1931年卡尔·博施因改进合成氨的方法获得诺贝尔化学奖,
2007年格哈德·埃特尔因发现了哈伯-博施法合成氨的作用机理获得诺贝尔化学奖。 和
在固体催化剂(Fe)表面合成氨的过程可用下图表示:
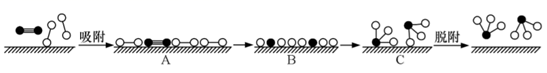
(图中 ![]() 、
、 ![]() 、
、 ![]() 、
、 ![]() 分别表示
分别表示 、
、
和固体催化剂);反应历程如下(*表示吸附态):
吸附: ;
。
表面反应: ;
;
。
脱附: 。
其中, 的吸附分解反应活化能高、反应速率慢,决定了合成氨的整体反应速率。
知识点

参考答案
采纳过本试题的试卷