试题详情
K2Cr2O7溶液中存在多个平衡。在考虑平衡:① (aq) +H2O(l)
(aq) +H2O(l) 2
2 (aq) K1=3.0× 10-2(25℃);②
(aq) K1=3.0× 10-2(25℃);② (aq)
(aq)
 (aq) +H+(aq) K2=3.3× 10-7(25℃)的条件下,25℃时,向0.10 mol/L K2Cr2O7溶液中加入NaOH,溶液中
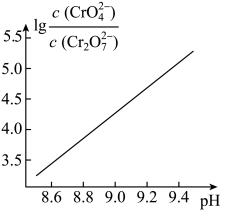
(aq) +H+(aq) K2=3.3× 10-7(25℃)的条件下,25℃时,向0.10 mol/L K2Cr2O7溶液中加入NaOH,溶液中 , 随pH的变化关系如图所示,溶液体积变化可忽略。下列说法中正确的是
, 随pH的变化关系如图所示,溶液体积变化可忽略。下列说法中正确的是
- A、已知Ka1(H2SO3) = 1.29× 10-2 , 由②可知向K2CrO4溶液中通SO2可制得KHCrO4
- B、
的值随溶液 pH的增大逐渐减小
- C、当溶液pH=9时,溶液中的
平衡浓度约为6 × 10-4mol/L
- D、当溶液pH=7时,c(K+) =c (
) +c(
) +2c (
)
知识点

参考答案