选择题
一定温度下:在  的四氯化碳溶液(
的四氯化碳溶液(  )中发生分解反应:
)中发生分解反应:  。在不同时刻测量放出的
。在不同时刻测量放出的  体积,换算成
体积,换算成  浓度如下表:
浓度如下表:
| | 0 | 600 | 1200 | 1710 | 2220 | 2820 | x |
| | 1.40 | 0.96 | 0.66 | 0.48 | 0.35 | 0.24 | 0.12 |
下列说法正确的是( )
- A、
,生成
的平均速率为
- B、 反应
时,放出的
体积为
(标准状况)
- C、 反应达到平衡时,
- D、 推测上表中的x为3930
利用 可消除
可消除 污染,反应原理为
污染,反应原理为 , 在10L密闭容器中分别加入
, 在10L密闭容器中分别加入 和
和 , 测得不同温度下
, 测得不同温度下 随时间变化的有关实验数据见下表。
随时间变化的有关实验数据见下表。
组别 | 温度/K | 时间/min 物质的量/mol | 0 | 10 | 20 | 40 | 50 |
① | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 | ||
② | 0.50 | 0.30 | 0.18 | M | 0.15 |
下列说法不正确的是( )
- A、 该反应为放热反应
- B、 组别①中0~10min内,
的平均反应速率为
- C、 若组别②改为恒压装置,则M值一定大于0.15
- D、 当有1molC-H键断裂同时有1molO-H键断裂,则达到平衡状态
某实验团队研究合成氨在不同条件下进行反应,平衡时氨气的含量与起始氢氮比 之间的关系如下图。下列说法正确的是( )
之间的关系如下图。下列说法正确的是( )

- A、
<420℃
- B、 b点时的转化率:
- C、 a、b、c、d四点对应的平衡常数由大到小的顺序为
- D、 工业合成氨一般以α-铁触媒为催化剂,400~500℃下反应,选取该温度的主要原因是氨的平衡产率更高
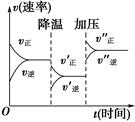
在某一恒温容积可变的密闭容器中发生反应:A(g)+B(g) 2C(g)。反应速率随时间的变化如图所示。下列说法正确的是( )
2C(g)。反应速率随时间的变化如图所示。下列说法正确的是( )

- A、 0~t2时,v正>v逆
- B、 t2时刻改变的条件是向密闭容器中加入C
- C、 Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ>Ⅱ
- D、 Ⅰ、Ⅱ两过程达到平衡时,平衡常数KⅠⅡ
一定条件下,向一带活塞、有钒触媒的密闭容器中充入 和
和 , 发生反应:
, 发生反应:
 , 则下列说法正确的是( )
, 则下列说法正确的是( )
- A、 该反应的逆方向低温自发
- B、 若容器绝热,则化学反应速率会越来越快
- C、 保持温度不变,达到平衡后,充入
,
的转化率将减小
- D、
不变,则该可逆反应已达到平衡状态
在373K时,把0.5molN2O4气通入体积为5L的恒容真空密闭容器中立即出现红棕色,反应进行到2s时,NO2的浓度为0.02mol/L,在60s时体系达到平衡,此时容器内压强为开始压强的1.6倍。下列说法正确的是( )
- A、 前2svN2O4=0.01mol/L·s
- B、 2s时体系内压强为开始时的1.1倍
- C、 平衡时体系内含N2O40.25mol
- D、 平衡时若压缩容器体积可提高N2O4的转化率
利用CO生产甲醇的反应为2H2(g)+CO(g)=CH3OH(g).在密闭容器中按物质的量之比为2:1充入H2和CO,测得平衡混合物中CH,OH的体积分数在不同压强下随温度的变化情况如图所示。
已知:①v正=k正·x(CO)·x2(H2),v逆=k逆·x(CH3OH),其中v正、逆为正、逆反应速率,k正、k逆·为速率常数,x为各组分的体积分数。
②K,为以分压表示的平衡常数,气体分压=气体总压x体积分数
下列相关说法错误的是( )

- A、 该反应的ΔH<0
- B、 B点与C点的平衡常数关系为KB=Kc
- C、 增大体系压强,k正-k逆·的值将增大
- D、 C点对应的平衡常数
在温度T1和T2时,分别将0.50 mol A和1.2 mol B充入体积为3 L的恒容密闭容器中,发生如下反应:A(g)+2B(g)  2C(g)+D(g),测得n(A)随时间变化数据如下表,下列说法正确的是( )
2C(g)+D(g),测得n(A)随时间变化数据如下表,下列说法正确的是( )
| 温度 | 时间/min | 0 | 10 | 20 | 40 | 50 |
| T1 | n(A)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(A)/mol | 0.50 | 0.30 | 0.18 | …… | 0.15 |
- A、 温度:T1>T2
- B、 反应达到平衡状态时,容器内压强不再发生变化
- C、 在温度T1时,0~10 min用B表示的平均反应速率为0.005mol/(L·min)
- D、 保持其他条件不变,缩小反应容器体积,逆反应速率增大,正反应速率减小
常压下羰基化法精炼镍的原理为  。
。  时,该反应的平衡常数
时,该反应的平衡常数  。
。
已知: 的沸点为
,固体杂质不参与反应。
第一阶段:将粗镍与 反应转化成气态
;
第二阶段:将第一阶段反应后的气体分离出来,加热至 制得高纯镍。
下列判断正确的是( )
- A、
是离子化合物
- B、 第一阶段,反应体系的温度应控制在
以上,以达到气化分离的目的
- C、 反应达到平衡状态以后,保持体积不变通入
,平衡正向移动,反应的平衡常数增大
- D、 第二阶段,可以通过增大压强来提高
分解率
二氧化碳催化加氢合成乙烯是综合利用 CO2的热点研究领域,对节能减排有重要意义。已知反应:6H2(g)+2CO2(g)  CH2=CH2(g)+4H2O(g),温度对 CO2的平衡转化率和催化剂催化效率的影响如图所示,下列说法错误的是( )
CH2=CH2(g)+4H2O(g),温度对 CO2的平衡转化率和催化剂催化效率的影响如图所示,下列说法错误的是( )

- A、 正反应为放热反应
- B、 化学平衡常数:KM>KN
- C、 当温度高于 250 ℃时,催化剂的催化效率降低是因为平衡逆向移动引起的
- D、 若初始投料比n(H2)∶n(CO2)=3∶1,则图中 M 点的乙烯体积分数约为 7.7%
用  代替
代替  与燃料
与燃料  反应是一种清洁的新型燃烧技术,发生如下反应:
反应是一种清洁的新型燃烧技术,发生如下反应:
①
②
③
下列说法正确的是( )
- A、 ①和②是主反应,反应③是副反应
- B、 反应③达到平衡后压缩容器体积,再次平衡时平衡常数增大
- C、 反应②达到平衡后充入适量
,再次平衡时
的物质的量增大
- D、
的反应热
向某恒容密闭容器中加入1.6 mol • L-1的NO2后,会发生如下反应:2NO2(g)⇌N2O4(g) △H =-56.9kJ•mol-1。其中N2O4的物质的量浓度随时间的变化如图所示,下列说法错误的是( )

- A、 升高温度,60s后容器中混合气体颜色加深
- B、 0-60s内,NO2的转化率为75%
- C、 0-60s内,v(NO2)=0.02mol• L-1• s-1
- D、 a、b两时刻生成NO2的速率v(a)>v(b)
CH4—CO2催化重整可以得到合成气(CO和H2),有利于减小温室效应,其主要反应为CH4(g)+CO2(g)⇌ 2CO(g)+2H2(g) ΔH=+247 kJ·mol−1 , 同时存在以下反应:积碳反应:CH4(g) ⇌C(s) +2H2(g) ΔH=+75 kJ·mol−1;消碳反应:CO2(g) +C(s) ⇌2CO(g) ΔH=+172 kJ·mol−1 , 积碳会影响催化剂的活性,一定时间内积碳量和反应温度的关系如下图。

下列说法正确的是( )
- A、 高压利于提高CH4的平衡转化率并减少积碳
- B、 增大CO2与CH4的物质的量之比有助于减少积碳
- C、 温度高于600℃,积碳反应的化学反应速率减慢,消碳反应的化学反应速率加快,积碳量减少
- D、 升高温度,积碳反应的化学平衡常数K减小,消碳反应的K增大
反应 2A  B+D 在四种不同条件下进行,B、D 起始浓度为零,A 的浓度(mol•L—1)随反应时间(min)的变化情况如下表:
B+D 在四种不同条件下进行,B、D 起始浓度为零,A 的浓度(mol•L—1)随反应时间(min)的变化情况如下表:

下列说法正确的是( )
- A、 在实验 1,反应在 10 至 20 分钟时间内物质 A 的平均速率为 0.013mol/(L•min)
- B、 在实验 2,A 的初始浓度 C2>1.0mol•L-1
- C、 设实验 3 的反应速率为v3 , 实验 1 的反应速率为v1 , 则v3<v1
- D、 实验 4 中,该反应在 30min 后才达到平衡状态
在100℃时,容积为5L的真空密闭容器中加入一定量的N2O4 , 容器内N2O4和NO2的物质的量变化如下表所示:
| 时间/s | 0 | 2 | 10 | 30 | 60 | 90 |
| n(N2O4)/mol | 0.3 | 0.25 | 0.15 | 0.125 | b | 0.12 |
| n(NO2)/mol | 0 | 0.1 | a | 0.35 | 0.36 | 0.36 |
下列说法正确的是( )
- A、 10s时,以NO2浓度变化表示的该反应速率为0.006mol•L•-1•s-1
- B、 该温度下反应2(NO2g)⇌N2O4(g)的平衡常数K=0.216
- C、 35s时容器内压强为反应前的1.6倍
- D、 其它条件不变,90s后向容器中再加入0.3molNO2建立新平衡时,与原平衡时比较,气体平均相对分子质量增大
工业上常用铁碳混合物处理含Cu2+废水获得金属铜。当保持铁屑和活性炭总质量不变时,测得废水中Cu2+浓度在不同铁碳质量比(x)条件下随时间变化的曲线如下图所示。

下列推论不合理的是( )
- A、 活性炭对Cu2+具有一定的吸附作用
- B、 铁屑和活性炭会在溶液中形成微电池,铁为负极
- C、 增大铁碳混合物中铁碳比(x),一定会提高废水中Cu2+的去除速率
- D、 利用铁碳混合物回收含Cu2+废水中铜的反应原理:Fe+Cu2+=Fe2++Cu
已知反应  ,不同温度下,容器中
,不同温度下,容器中  浓度与反应时间的关系如图所示,下列说法正确的是( )
浓度与反应时间的关系如图所示,下列说法正确的是( )

- A、
- B、
点的正反应速率大于
点的逆反应速率
- C、
点的反应速率小于
点的反应速率
- D、
点时
的浓度为
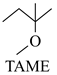 △H1
△H1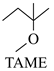 △H2
△H2