选择题
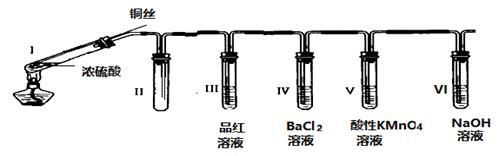
若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是( )

- A、
与浓硫酸反应,只体现
的酸性
- B、 a处变红,说明
是酸性氧化物
- C、 b或c处褪色,均说明
具有漂白性
- D、 试管底部出现白色固体,说明反应中无
生成
下列关于硫酸的说法正确的是( )
- A、 常温下,可用铁片与浓硫酸制取
- B、 实验室用98%的浓硫酸与
固体制取
- C、 实验室制备乙烯时,浓硫酸与乙醇的体积投料比约为3:1
- D、 等质量的水和发烟硫酸(
)混合后所得溶质质量分数为50%
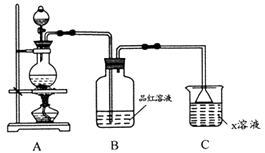
用图所示装置探究铜丝(下端卷成螺旋状)与过量浓硫酸的反应。

现象:试管①中液面上方有白雾,底部有灰白色固体。
下列实验不合理的是( )
- A、 浸
溶液的棉团用于吸收多余的
- B、 加热、将铜丝下端卷成螺旋状能提高
的生成速率
- C、 ②中用石蕊溶液验证
水溶液的酸性,③中用品红溶液验证
的生成
- D、 冷却后,将①中物质倒入盛有水的另一支试管,以确认
的生成
铜与浓硫酸反应的装置如图所示。下列描述合理的是( )
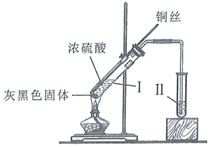
- A、 反应过程中,试管Ⅰ中出现灰黑色固体是
- B、 反应结束后,为观察溶液颜色需向试管Ⅰ中加入水
- C、 若试管Ⅱ盛放紫色石蕊溶液,可观察到紫色褪至无色
- D、 为验证气体产物具有还原性,试管Ⅱ可盛放溴水
利用Cu和浓硫酸制备SO2的反应涉及的装置,下列说法正确的是()
- A、 用装置①制备SO2

- B、 用装置②检验和收集SO2

- C、 用装置③稀释反应后溶液

- D、 用装置④测定反应后溶液中c(H+)

下列说法错误的是( )
- A、 聚氯乙烯可以制食物保鲜膜
- B、 铝热反应可用于焊接钢轨
- C、 液氯可以保存在钢瓶中
- D、 常温下可用铁槽车运输浓硫酸
用下列实验装置完成对应的实验,能达到实验目的的是( )
实验装置 |
|
|
|
|
实验目的 | 实验验证浓硫酸具有脱水性、氧化性 | 制取并收集少量氨气 | 验证NaHCO3和Na2CO3的热稳定性 | 采用CCl4萃取I2 |
A | B | C | D |
- A、 A
- B、 B
- C、 C
- D、 D
浓硫酸与蔗糖反应的实验,对现象的解释不合理的是( )
| 选项 | 现象 | 解释 |
| A | 蔗糖变黑 | 浓硫酸具有脱水性 |
| B | 有刺激性气味 | 浓硫酸具有强酸性 |
| C | 固体体积膨胀 | 生成大量气体 |
| D | 烧杯壁发烫 | 反应放热 |
- A、 A
- B、 B
- C、 C
- D、 D
将适量蔗糖放入烧杯中,滴几滴水,搅拌均匀;然后再加入适量浓硫酸,迅速搅拌,观察到蔗糖逐渐变黑,体积膨胀,并产生气体,下列说法错误的是
- A、 浓硫酸表现出脱水性和强氧化性
- B、 黑色物质是炭
- C、 浓硫酸被氧化
- D、 气体中含有SO2和CO2
下列鉴别浓硫酸和稀硫酸的操作与结论有误的是( )
操作 | 结论 | |
A | 分别加入金属铝片 | 产生刺激性气味者为浓硫酸 |
B | 分别加入到盛水的试管中 | 剧烈放热者为浓硫酸 |
C | 取等体积样品,称量质量 | 质量大者为浓硫酸 |
D | 分别滴在火柴梗上 | 变黑者为浓硫酸 |
- A、 A
- B、 B
- C、 C
- D、 D
硫酸工业生产中,为有利于 的转化且充分利用能量。在热交换器接触室中装有热交换器(如图),温度最低的是( )
的转化且充分利用能量。在热交换器接触室中装有热交换器(如图),温度最低的是( )

- A、 a处
- B、 b处
- C、 c处
- D、 d处
下列有关硫酸的叙述正确的是( )
- A、 常温下铜与浓硫酸剧烈反应
- B、 盛有浓硫酸的试剂瓶敞口放置,瓶口会出现大量白雾
- C、 将浓硫酸和稀硫酸分别滴入蔗糖中会产生不同现象
- D、 浓硫酸有强氧化性,常温下不能用铁制或铝制容器盛装
探究金属铜与过量浓硫酸反应的装置(固定装置已略去)如图所示。关于实验操作或现象述不正确的是( )

- A、 上下抽动铜丝,可控制反应随时发生或停止
- B、 c装置中黑色固体变为红色
- C、 e中可以选用NaOH溶液或酸性KMnO4溶液
- D、 其他条件不变,用铁丝代替铜丝,c、d中两次实验现象相同
用25mL18.4mol/L的浓硫酸与铜共热一段时间后,冷却,过滤除去多余的铜,将滤液稀释到100 mL,所得溶液中SO42-浓度为3mol/L,则此时溶液中CuSO4的物质的量浓度为( )
- A、 0.5mol/L
- B、 1.6 mol/L
- C、 1.8 mol/L
- D、 3mol/L
加热条件下,20 mL 18 mol/L的浓H2SO4与过量的碳反应,可得到标况下的CO2( )
- A、 小于4.032L
- B、 等于4.032L
- C、 大于4.032L
- D、 无法确定