试题详情
某兴趣小组在实验室发现一瓶敞口放置的氧化钙,猜测该氧化钙可能变质。小明为确定该瓶氧化钙的成分进行了实验探究,如下表所示:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量该氧化钙样品于烧杯中,加水搅拌,静置,取上层清液滴加到红色石蕊试纸上 | ①烧杯壁变热,石蕊试纸变为蓝色 | 样品中含有氧化钙和氢氧化钙 |
| ②烧杯底部有白色固体 | 样品中含有碳酸钙 |
【交流讨论】小组讨论后,同学们认为:“现象”不足以证明样品中有氢氧化钙,原因是(用化学方程式表示);“现象②”不足以证明样品中有碳酸钙,原因是。
兴趣小组同学为准确测定该瓶氧化钙的成分,进行了如下探究。
【提出问题】该瓶氧化钙中都有哪些成分,各成分的质量比是多少?
【查阅资料】氢氧化钙在一定温度下能分解:
碱石灰是氢氧化钠与氧化钙的固体混合物,能吸收水和二氧化碳
【设计并实施实验】兴趣小组设计了如图所示的实验(装置气密性良好)。取该氧化钙样品放在装置B的玻璃管中,先通入一会空气,再称量C、D装置的质量,然后边通入空气,边用酒精喷灯加热(能达到
高温),至固体不再发生变化,继续通一会空气,实验后测得
装置增重
, D装置增重
。
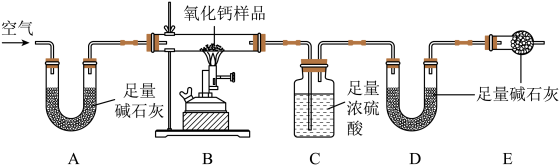
【形成结论】该氧化钙样品中的成分是,它们的质量比是。
【反思评价】装置的作用是。如果没有
装置,可能会导致氧化钙样品成分中的测定结果偏大。
【拓展应用】为废物利用,兴趣小组打算用这瓶变质的氧化钙与足量的稀盐酸反应,再蒸发制取产品氯化钙固体,与变质前的氧化钙相比,变质后的氧化钙对产品氯化钙的产量是否会有影响,为什么?。
知识点

参考答案
采纳过本试题的试卷