选择题
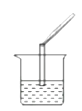
下列实验操作正确的是( )
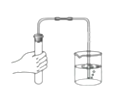
- A、 检查装置气密性
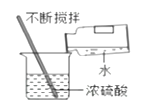
- B、 稀释浓硫酸
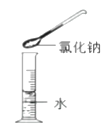
- C、 配制氯化钠溶液
- D、 测定溶液pH值
金属材料在人类活动中已得到越来越广泛的应用。下列属于金属共性的是 ( )
- A、 很高的熔点
- B、 良好的导电性
- C、 很大的硬度
- D、 银白色的光泽
下列每组物质(主要成分)的名称、俗称、化学式三者不能表示同一种物质的是( )
- A、 氯化钠、食盐、NaCl
- B、 硫酸铜晶体、胆矾、CuSO4·5H2O
- C、 碳酸钠、纯碱、Na2CO3
- D、 碳酸钙、熟石灰、Ca(OH)2
小李家地处少雨的高寒山区,种的庄稼生长不茂盛,叶色偏黄,且籽粒不饱满,小李学了化学知识后,帮助父母科学种田,建议父母买化肥改善现状,以获得好收成,他应向父母提出买的化肥是( )
- A、 CO(NH2)2
- B、 KNO3
- C、 Ca2(PO4)3
- D、 NH4H2PO4
下列各组物质在pH=3水溶液中能大量共存的是( )
- A、 AgNO3 , NaCl
- B、 Na2SO4 , MgCl2
- C、 NaCl,Na2CO3
- D、 MgCl2 , KOH
高铁酸钾(K2FeO4)是具有紫色光泽的微细结晶粉末,它的氧化性超过高锰酸钾,是一种集氧化、吸附、杀菌、灭藻的新型、高效的多功能水处理剂。干燥的高铁酸钾在198℃以下是稳定的,受热易分解为氧化铁、金属氧化物和氧气。根据以上信息,下列说法不正确的是( )
- A、 保存高铁酸钾时应注意防潮避热
- B、 高铁酸钾是一种化合物
- C、 高铁酸钾中铁元素的化合价为+6价
- D、 高铁酸钾的氧化性属于物理性质
下列各物质,能按照“溶解—过滤—蒸发”的操作步骤加以分离的是( )
- A、 氧化铜和硫酸铜
- B、 氯化钠和硝酸钾
- C、 酒精和水
- D、 氧化铁和铁
归纳和演绎是重要的科学方法。下列归纳和演绎合理的是( )
- A、 有机物是一类含碳化合物,所以CH4、CO2 都是有机物
- B、 硫酸、盐酸电离时都能产生H+ , 所以 电离时能产生H+的化合物是酸
- C、 金属Fe、Zn能与酸反应生成氢气,所以金属都能与酸反应生成氢气
- D、 氧化物是由两种元素组成,其中一种是氧元素的化合物,所以水是氧化物
现有① NaOH溶液、② KCl溶液、③ MgCl2溶液、④ CuSO4溶液,不用其他试剂,可通 过实验方法将它们一一鉴别开来,鉴别出来的先后顺序可能是( )
- A、 ①②③④
- B、 ①④③②
- C、 ④③②①
- D、 ④①③②
在稀硫酸中分别加入下列物质,反应现象符合的是( )
- A、 铜片:看到铜片周围有气泡产生
- B、 氧化铁:固体消失,溶液变成浅绿色
- C、 氯化钡:无明显现象
- D、 碳酸钠溶液: 产生气泡
滴有酚酞的氢氧化钡溶液与下列各种物质恰好完全反应后,溶液仍显红色的是( )
- A、 H2SO4
- B、 HNO3
- C、 K2CO3
- D、 CO2
下列物质在敞口容器中久置,因发生化学变化溶液质量减小的是( )
- A、 浓硫酸
- B、 浓盐酸
- C、 氢氧化钠溶液
- D、 石灰水
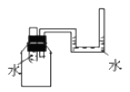
如图,实验室中用碳酸钙与盐酸反应制取CO2气体,此CO2气体中常含有水蒸气和氯化氢气体,若要除去这两种气体杂质,可将生成的气体通过甲、乙两个洗气瓶,通过导管的正确顺序是 ( )

- A、 ①②③④
- B、 ③④②①
- C、 ②①③④
- D、 ④③②①
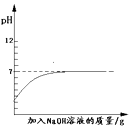
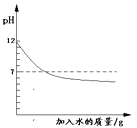
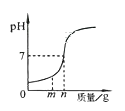
下列实验对应的图像正确的是 ( )
| A | B | C | D |
| 向稀硫酸中加入过量的锌,溶液中溶质质量 | 向pH=2的盐酸中滴加过量的氢氧化钠溶液 | 向盐酸和氯化铁的混合溶液中加入过量的氢氧化钠溶液 | 向pH=12的氢氧化钠溶液中加水稀释 |
|
|
|
|
|
- A、 A
- B、 B
- C、 C
- D、 D
用NaCl、CaCl2、AlCl3溶液分别与同一AgNO3溶液反应,生成等质量的AgCl沉淀,则消耗AgNO3溶液的质量比为( )
- A、 1:1:1
- B、 1:2:3
- C、 3:2:1
- D、 6:3:2
如图,在盛有一定质量分数稀盐酸的容器中,放一塑料方块,漂浮于稀盐酸中,若向容器中加入足量石灰石(CaCO3)使其与盐酸完全反应后,则塑料方块在溶液中( )

- A、 下沉
- B、 上浮
- C、 不变
- D、 无法判断


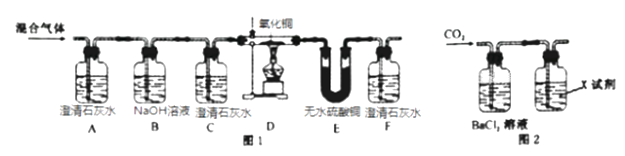 (查阅资料可知:CuO+H2
(查阅资料可知:CuO+H2