单选题
常温下,次氯酸电离平衡体系中各成分的组成分数 
 为
为  或
或  ]与
]与  的关系如图所示。下列有关说法正确的是( )
的关系如图所示。下列有关说法正确的是( )
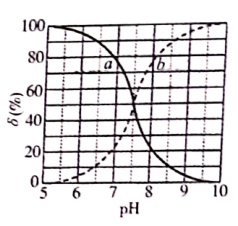
- A、 次氯酸的电离方程式为
- B、 曲线
依次表示
、
的变化
- C、 次氯酸电离常数
的数量级为
- D、 向次氯酸溶液中加
溶液,
将减小
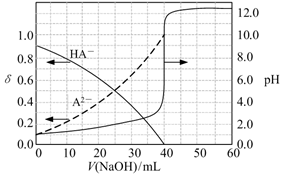
常温下,以酚酞作指示剂,用0.1mol/L的NaOH溶液滴定20.00mL0.1mol/L的二元酸H2A溶液。溶液中pH、分布系数δ随滴加NaOH溶液体积V(NaOH)的变化关系如图所示,有关说法正确的是 ( )
已知:A2−的分布系数为
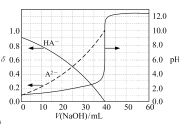
- A、 当V(NaOH)=0mL时,c(H2A)>c(HA- )>c(A2- )>c(H+)>c(OH- )
- B、 当V(NaOH)=20.00mL时,c(Na+)<c(HA- )+2c(A2- )
- C、 室温下,HA-的电离常数值为1.0×10-5
- D、 当V(NaOH)=40.00mL时,c(HA -)+c(H+)=c(A2- )+c(OH- )
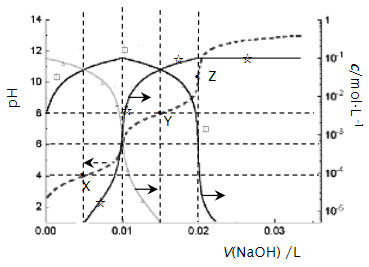
常温下,向0.01 mol∙L-1的一元酸HX溶液中通入氨气,此过程混合溶液中  与pH之间关系如图所示(忽略溶液的体积变化)。下列叙述正确的是( )
与pH之间关系如图所示(忽略溶液的体积变化)。下列叙述正确的是( )
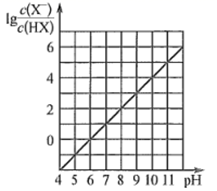
- A、 pH=7时,溶液中c(
)=
mol∙L-1
- B、 常温下,K(HX)≈1×10- 5
- C、 当溶液为碱性时,c(X- )<c(HX)
- D、 混合溶液中不可能在:c(X-)>c(
)>c(H+)>c(OH-)
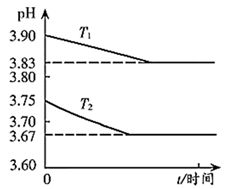
25℃时,HF和HCN的电离平衡常数Ka分别为6.8×10-4、6.2×10-10 , 稀释HF、HCN的稀溶液时,溶液pH随加水量的变化如图所示,下列说法中正确的是( )
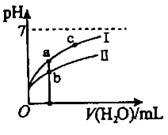
- A、 a点所示溶液中c(H+)=c(CN-)+c(OH-)
- B、 a、b、c三点所示溶液中水的电离程度c>a>b
- C、 向NaCN溶液中滴加HF溶液的离子方程式:CN-+H+=HCN
- D、 同浓度NaF和NaCN的混合溶液中: c(Na+)>c(CN-)>c(F-)> c(OH -)> c(H+)
常温下,对于pH=9的CH3COONa溶液,下列说法错误的是( )
- A、 该溶液中:c(OH-)>c(CH3COOH)+c(H+)
- B、 往该溶液中滴加醋酸,可能出现c(Na+) <c(CH3COO- )
- C、 往该溶液中通入HCl气体,
保持不变
- D、 相同温度下,该CH3COONa溶液的浓度大于pH=9的NaOH溶液的浓度
关于常温下pH均为3的盐酸和醋酸两种溶液,下列说法正确的是( )
- A、 醋酸溶液的物质的量浓度小于盐酸
- B、 将醋酸溶液稀释至原体积的10倍,所得溶液pH<4
- C、 c(Cl-)=c(CH3COOH)+c(CH3COO-)
- D、 相同体积的两种酸,分别与足量镁条反应,盐酸产生的气体多
NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的Ka1=1.1×10-3 , Ka2=3.9×10-6) 溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是( )
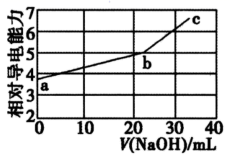
- A、 混合溶液的导电能力与离子浓度和种类有关
- B、 Na+与A-的导电能力之和大于HA-的导电能力
- C、 b点的混合溶液pH=7
- D、 c点的混合溶液中,c(Na+)>c(K+)>c(A2-)>c(OH-)
常温下,下列溶液的离子浓度关系式正确的是( )
- A、 pH=4的醋酸溶液稀释10倍,溶液中c(CH3COOH)、c(OH-)均减小
- B、 等物质的量浓度的①H2CO3②NaHCO3③(NH4)2CO3三种溶液的c(CO
)的大小关系为③>①>②
- C、 CH3COONa溶液的pH=8,则c(Na+)-c(CH3COO-)=9.9×10-7mol·L-1
- D、 0.1mol·L-1的氨水pH=a,0.01mol·L-1的氨水pH=b,则a-l=b
下列过程与“盐类的水解平衡”或“难溶电解质的溶解平衡”无关的是( )
- A、 将NaOH溶液加入NaHSO4溶液中使其转化为Na2SO4
- B、 将TiCl4加入水中并加热使其转化为TiO2•xH2O
- C、 将Na2CO3溶液加入水垢中使CaSO4转化为CaCO3
- D、 将Na2S溶液加入含Hg2+的废水中使其转化为HgS沉淀
向NaOH溶液中缓慢通入CO2气体,溶液中CO  的物质的量与通入CO2物质的量的关系如图。下列关于图中a、b、c三点溶液的说法错误的是( )
的物质的量与通入CO2物质的量的关系如图。下列关于图中a、b、c三点溶液的说法错误的是( )
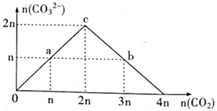
- A、 a、b、c三点溶液都满足:c(Na+)+c(H+)=c(HCO
)+2c(CO
)+c(OH-)
- B、 a、b、c三点溶液中水的电离程度:a=b<c
- C、 a、b两点溶液的pH满足:pH(a)>pH(b)
- D、 b点溶液满足:c(Na+)>c(HCO
)>c(CO
)>c(OH-)>c(H+)
常温下,向含少量盐酸的0.1mol/L的CrCl3溶液中逐滴滴加NaOH溶液,所加NaOH溶液的体积与溶液pH变化如图所示。
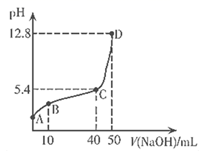
已知:Cr(OH)3为灰绿色的沉淀,当Cr3+浓度为10-5mol/L时,可认为沉淀完全,碱过量时生成[Cr(OH)4]-离子。下列说法正确的是( )
- A、 AB段发生反应的离子方程式为:
- B、 A到D过程中,溶液中水的电离程度先减小后增大
- C、 当溶液pH=5时,
- D、 D点溶液中
反应CO2 + 2NaOH = Na2CO3 + H2O可用于捕捉废气中的CO2 , 下列表示或说法正确的是( )
- A、 NaOH的电子式:
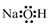
- B、 中子数为8的碳原子:
- C、 CO
的空间构型:平面三角形
- D、 CO
的水解方程式:CO
+2H2O
H2CO3+2OH−
室温下,通过下列实验探究FeCl3水解反应[FeCl3(黄色)+3H2O⇌Fe(OH)3(红褐色)+3HCl]的条件。
| 实验序号 | 实验操作 | 实验现象 |
| 1 | 将FeCl3溶液加热片刻 | 溶液颜色变深 |
| 2 | 向FeCl3 溶液中通入少量HCl气体 | 溶液颜色变浅 |
| 3 | 向FeCl3溶液中加入少量(NH4)2SO4固体 | 溶液颜色变浅 |
| 4 | 向FeCl3溶液中加入少量NaHCO3固体 | 产生红褐色沉淀,溶液中出现大量气泡 |
下列有关说法正确的是( )
- A、 实验1得到的溶液中有c(Cl-)>c(Fe3+)>c(OH-)>c(H+)
- B、 实验2中FeCl3水解反应的化学平衡常数变小
- C、 实验3得到的溶液中有3c(Fe3+)+c(H+)=c(NH3·H2O)+c(Cl-)+c(OH-)
- D、 实验4中反应的离子方程式为Fe3++
+H2O=Fe(OH)3↓+CO2↑
根据下列图示所得出的结论错误的是( )
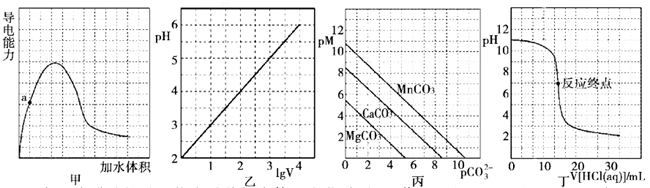
- A、 图甲表示冰醋酸的导电能力随着加水体积变化关系图,若用湿润的
试纸测量a点的
,则测量结果可能偏小
- B、 图乙表示
的盐酸溶液加水稀释至
随
的变化关系图
- C、 图丙表示一定温度下三种碳酸盐
的沉淀溶解平衡曲线图
,则有
、
、
的
依次减小
- D、 图丁表示
盐酸滴定
溶液的滴定曲线
下列有关说法正确的是( )
- A、 氧化钾溶于水能导电,所以氧化钾是电解质
- B、 强电解质一定是含有离子键,弱电解质中一定含弱极性共价键
- C、 酸性氧化物不一定是非金属氧化物,碱性氧化物都是金属氧化物
- D、 纳米铁粉分散在水中形成胶体,可以通过吸附的方式高效地去除被污染水体中的
、
、
、
等重金属离子