选择题
某温度下,在恒容密闭容器中加入一定量X,发生反应  ,一段时间后达到平衡。下列说法错误的是( )
,一段时间后达到平衡。下列说法错误的是( )
- A、 升高温度,若
增大,则
- B、 加入一定量Z,达新平衡后
减小
- C、 加入等物质的量的Y和Z,达新平衡后
增大
- D、 加入一定量氩气,平衡不移动
某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度及时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是( )

- A、 其他条件相同时,催化剂浓度越大,反应速率越大
- B、 其他条件相同时,降冰片烯浓度越大,反应速率越大
- C、 条件①,反应速率为
- D、 条件②,降冰片烯起始浓度为
时,半衰期为
制备水煤气的反应 
 ,下列说法正确的是( )
,下列说法正确的是( )
- A、 该反应
- B、 升高温度,反应速率增大
- C、 恒温下,增大总压,H2O(g)的平衡转化率不变
- D、 恒温恒压下,加入催化剂,平衡常数增大
Li电池使用过程中会产生LiH,对电池的性能和安全性带来影响。可用D2O与LiH进行反应测定LiH含量,由产物中的n(D2)/n(HD)比例可推算n(Li)/n(LiH)。
已知:①2LiH⇌2Li+H2 △H>0
②LiH+H2O=LiOH+H2↑
下列说法错误的是( )
- A、 H2O、D2O的化学性质基本相同
- B、 Li与D2O反应的方程式是2Li+2D2O=2LiOD+D2↑
- C、 n(D2)/n(HD)比例小说明n(Li)/n(LiH)比例大
- D、 80℃下的n(D2)/n(HD)大于25℃下的n(D2)/n(HD)
已知C3H8脱H2制烯烃的反应为C3H8 = C3H6+H2。固定C3H8浓度不变,提高CO2浓度,测定出口处C3H6、H2、CO浓度。实验结果如下图。

已知:
C3H8(g)+5O2(g)=3CO2(g)+4H2O(g) △H=-2043.9kJ/mol
C3H6(g)+9/2O2(g)=3CO2(g)+3H2O(g) △H=-1926.1kJ/mol
H2(g)+1/2O2(g)=H2O(g) △H=-241.8kJ/mol
下列说法错误的是( )
- A、 C3H8(g)=C3H6(g)+H2(g) △H=+124kJ/mol
- B、 C3H6、H2的浓度随CO2浓度变化趋势的差异是因为发生了CO2+H2
CO+H2O
- C、 相同条件下,提高C3H8对CO2的比例,可以提高C3H8的转化率
- D、 如果生成物只有C3H6、CO、H2O、H2 , 那么入口各气体的浓度c0和出口各气体的浓度符合3c0(C3H8)+c0(CO2)=3c(C3H6)+c(CO)+3c(C3H8)+c(CO2)
NO2和N2O4存在平衡:2NO2(g)⇌N2O4(g) △H<0。下列分析正确的是( )
- A、 1 mol平衡混合气体中含1 mol N原子
- B、 断裂2 mol NO2分子中的共价键所需能量小于断裂1 mol N2O4中的共价键所需能量
- C、 恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的
- D、 恒容时,水浴加热,由于平衡正向移动导致气体颜色变浅
一定温度下:在  的四氯化碳溶液(
的四氯化碳溶液(  )中发生分解反应:
)中发生分解反应:  。在不同时刻测量放出的
。在不同时刻测量放出的  体积,换算成
体积,换算成  浓度如下表:
浓度如下表:
| | 0 | 600 | 1200 | 1710 | 2220 | 2820 | x |
| | 1.40 | 0.96 | 0.66 | 0.48 | 0.35 | 0.24 | 0.12 |
下列说法正确的是( )
- A、
,生成
的平均速率为
- B、 反应
时,放出的
体积为
(标准状况)
- C、 反应达到平衡时,
- D、 推测上表中的x为3930
相同温度和压强下,关于物质熵的大小比较,合理的是( )
- A、
- B、
- C、
- D、
化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是( )
| 选项 | 操作或做法 | 目的 |
| A | 将铜丝插入浓硝酸中 | 制备 |
| B | 将密闭烧瓶中的 | 探究温度对平衡移动的影响 |
| C | 将溴水滴入 | 萃取溶液中生成的碘 |
| D | 实验结束,将剩余 | 节约试剂 |
- A、 A
- B、 B
- C、 C
- D、 D
反应  经历两步:①
经历两步:①  ;②
;②  。反应体系中
。反应体系中  、
、  、
、  的浓度c随时间t的变化曲线如图所示。下列说法不正确的是( )
的浓度c随时间t的变化曲线如图所示。下列说法不正确的是( )

- A、 a为
随t的变化曲线
- B、
时,
- C、
时,
的消耗速率大于生成速率
- D、
后,
- A、
重水(
)中含有的质子数为
- B、
的
与
完全反应时转移的电子数为
- C、
环状
(
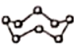 )分子中含有的
)分子中含有的 键数为
- D、
的
溶液中
离子数为
已知相同温度下,  。某温度下,饱和溶液中
。某温度下,饱和溶液中  、
、  、与
、与  的关系如图所示。
的关系如图所示。

下列说法正确的是( )
- A、 曲线①代表
的沉淀溶解曲线
- B、 该温度下
的
值为
- C、 加适量
固体可使溶液由a点变到b点
- D、
时两溶液中
常温下,用  的盐酸分别滴定20.00mL浓度均为
的盐酸分别滴定20.00mL浓度均为  三种一元弱酸的钠盐
三种一元弱酸的钠盐  溶液,滴定曲线如图所示。下列判断错误的是( )
溶液,滴定曲线如图所示。下列判断错误的是( )

- A、 该
溶液中:
- B、 三种一元弱酸的电离常数:
- C、 当
时,三种溶液中:
- D、 分别滴加20.00mL盐酸后,再将三种溶液混合:
铁的配合物离子(用  表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:
表示)催化某反应的一种反应机理和相对能量的变化情况如图所示:

下列说法错误的是( )
- A、 该过程的总反应为
- B、
浓度过大或者过小,均导致反应速率降低
- C、 该催化循环中
元素的化合价发生了变化
- D、 该过程的总反应速率由Ⅱ→Ⅲ步骤决定
室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v1=k1c2(M),反应②的速率可表示为v2=k2c2(M) (k1、k2为速率常数)。反应体系中组分M、Z的浓度随时间变化情况如图,下列说法错误的是( )

- A、 0~30min时间段内,Y的平均反应速率为6.67×10-8mol•L-1•min-1
- B、 反应开始后,体系中Y和Z的浓度之比保持不变
- C、 如果反应能进行到底,反应结束时62.5%的M转化为Z
- D、 反应①的活化能比反应②的活化能大



 (g) ∆H1<0
(g) ∆H1<0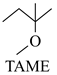 △H1
△H1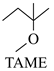 △H2
△H2 已知:25℃时,
已知:25℃时,