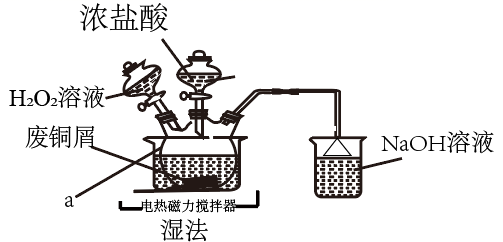
选择题
测定0.1mol·L-1Na2SO3溶液先升温再降温过程中的pH,数据如下。
时刻 | ① | ② | ③ | ④ |
温度/℃ | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比试验,④产生白色沉淀多。下列说法错误的是( )
- A、 Na₂SO3溶液中存在水解平衡:SO32-+H2O
HSO-3+OH-
- B、 ④的pH与①不同,是由于SO32-浓度减小造成的
- C、 ①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
- D、 ①与④的Kw值相等
某废水处理过程中始终保持H2S饱和,即 , 通过调节pH使
, 通过调节pH使 和
和 形成硫化物而分离,体系中
形成硫化物而分离,体系中 与
与 关系如下图所示,c为
关系如下图所示,c为 和
和 的浓度,单位为
的浓度,单位为 。已知
。已知 , 下列说法正确的是
, 下列说法正确的是

- A、
- B、 ③为
与
的关系曲线
- C、
- D、
- A、 相同温度下,等
的
和
溶液中,
- B、 将浓度均为
的
和
溶液加热,两种溶液的
均变大
- C、
时,
溶液与
溶液混合,测得
, 则此时溶液中
- D、
时,
的
溶液中加少量
固体,水的电离程度变小
下列实验中,均产生白色沉淀。
 下列分析错误的是( )
下列分析错误的是( )
- A、 Na2CO3与NaHCO3溶液中所含微粒种类相同
- B、 CaCl2能促进Na2CO3、NaHCO3水解
- C、 Al2(SO4)3能促进Na2CO3、NaHCO3水解
- D、 4个实验中,溶液滴入后,试管中溶液pH均降低
LiH2PO4是制备电池的重要原料。室温下,LiH2PO4溶液的pH随c初始(H2PO4–)的变化如图1所示,H3PO4溶液中H2PO4–的分布分数δ随pH的变化如图2所示,[  ]下列有关LiH2PO4溶液的叙述正确的是( )
]下列有关LiH2PO4溶液的叙述正确的是( )




- A、 溶液中存在3个平衡
- B、 含P元素的粒子有H2PO4–、HPO42–、PO43–
- C、 随c初始(H2PO4–)增大,溶液的pH明显变小
- D、 用浓度大于1 mol·L-1的H3PO4溶液溶解Li2CO3 , 当pH达到4.66时,H3PO4几乎全部转化为LiH2PO4
用0.100 mol·L-1 AgNO3滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所示。下列有关描述错误的是
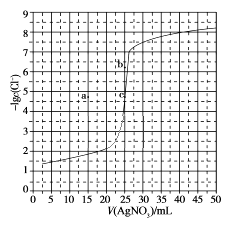
- A、 根据曲线数据计算可知Ksp(AgCl)的数量级为10-10
- B、 曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=Ksp(AgCl)
- C、 相同实验条件下,若改为0.0400 mol·L-1 Cl- , 反应终点c移到a
- D、 相同实验条件下,若改为0.0500 mol·L-1 Br- , 反应终点c向b方向移动
某化学兴趣小组在学习完温度对盐类水解的影响后,测定了0.1mol·L-1Na2CO3溶液的pH随温度的变化,结果如下图所示。下列分析正确的是( )

- A、 升温前溶液呈碱性的原因是:CO
+2H2O
H2CO3+2OH-
- B、 常温下,0.1 mol·L-1Na2CO3溶液中:c(Na+)>2c(CO
)+c(HCO
)
- C、 温度升高,Na2CO3水解程度增大,溶液pH增大,故图1实验数据一定不符合题意
- D、 降低温度,Na2CO3水解平衡移动和水的电离平衡移动对溶液pH的影响一致
粉煤灰含有50.19%的Al2O3、37.29%的SiO2 , 其余为Fe2O3、CaO等。粉煤灰“一步酸溶法”生产氧化铝的工艺流程如下图所示。下列叙述错误的是( )

- A、 “滤渣”的主要成分是二氧化硅
- B、 “树脂净化”的目的是将Al3+与Fe3+、Ca2+分离
- C、 “蒸发结晶”前应向氯化铝溶液中加入盐酸
- D、 循环使用X既降低成本,又防止污染环境
- A、 测溶液a的
, 证明
发生了水解
- B、 加入浓HCl,H+与Cl-对溶液颜色变化、Fe3+浓度大小的影响是一致的
- C、 向b中加入
后,黄色褪去,说明
能抑制
水解
- D、 将溶液a滴入沸水中,加热,检测有丁达尔效应,说明加热能促进
水解
实验室中下列做法错误的是( )
- A、 中和滴定时,滴定管用所盛装的溶液润洗2~3次
- B、 配制FeCl3溶液时,将FeCl3固体加入适量蒸馏水中,搅拌使其完全溶解
- C、 向容量瓶转移液体时,用于引流的玻璃棒接触容量瓶内壁刻度线以下
- D、 蒸馏完毕后,先停止加热,待装置冷却后,停止通水,再拆卸蒸馏装置
实验测得 10 mL 0. 50 mol•L -1NH4Cl溶液、10 mL 0. 50 mol•L -1CH3COONa溶液的pH分别随温度与稀释加水量的变化如图所示。已知25℃时CH3COOH和NH3•H2O的电离常数均为1. 8×10-5.下列说法错误的是( )
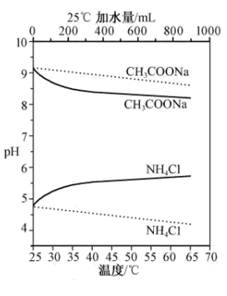
- A、 加水稀释初期两种盐的水解率变化程度比稀释后期大
- B、 图中虚线表示pH随加水量的变化,实线表示pH随温度的变化
- C、 将NH4Cl溶液加水稀释至浓度
mol・L-1溶液pH变化值小于lgx
- D、 将稀释相同倍数的NH4Cl与CH3COONa溶液混合,混合液中 c(CH3COO-)= c(NH
)
常温下,向0.01 mol∙L-1的一元酸HX溶液中通入氨气,此过程混合溶液中  与pH之间关系如图所示(忽略溶液的体积变化)。下列叙述正确的是( )
与pH之间关系如图所示(忽略溶液的体积变化)。下列叙述正确的是( )
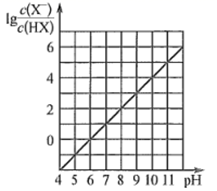
- A、 pH=7时,溶液中c(
)=
mol∙L-1
- B、 常温下,K(HX)≈1×10- 5
- C、 当溶液为碱性时,c(X- )<c(HX)
- D、 混合溶液中不可能在:c(X-)>c(
)>c(H+)>c(OH-)
25℃时,向20. 00 mL 0.1 mol/L H2X溶液中滴入0.1 mo1/L NaOH溶液,溶液中由水电离出的c水(OH-) 的负对数[一lgc水(OH-)]即pOH水-与所加NaOH溶液体积的关系如图所示。下列说法中正确的是( )

- A、 水的电离程度:M>P
- B、 图中P点至Q点对应溶液中
逐渐增大
- C、 N点和Q点溶液的pH相同
- D、 P点溶液中
下列说法正确的是( )
- A、 用苯萃取溴水中的Br2 , 分液时先从分液漏斗下口放出水层,再从上口倒出有机层
- B、 欲除去H2S气体中混有的HCl,可将混合气体通入饱和Na2S溶液
- C、 乙酸乙酯制备实验中,要将导管插入饱和碳酸钠溶液底部以利于充分吸收乙酸和乙醇
- D、 用pH试纸分别测量等物质的量浓度的NaCN和NaClO溶液的pH,可比较HCN和HClO的酸性强弱
将浓度均为0.1mol∙L-1的下列溶液稀释10倍,其中pH增大的是( )
- A、 HNO3
- B、 NaOH
- C、 KI
- D、 NaHCO3
用绿矾(FeSO4∙7H2O)配制FeSO4溶液, 常加入稀硫酸和( )
- A、 锌粉
- B、 铁粉
- C、 硫酸铁
- D、 盐酸
NA表示阿伏加德罗常数的值,下列说法正确的是( )
- A、 1mol硝基(-NO2)与46g二氧化氮(NO2)所含的电子数均为23NA
- B、 0.1mol/L(NH4)2SO4溶液与0.2 mol/LNH4Cl溶液中的NH4+数目相同
- C、 标准状况下,2.24L三氯甲烷中含碳氯共价键的数目为0.3NA
- D、 向FeI2溶液中通入适量Cl2 , 当有1 mol Fe2+被氧化时,转移的电子数为NA
下列关于物质结构和元素性质说法正确的是( )
- A、 非金属元素之间形成的化合物一定是共价化合物
- B、 乙醇可与水以任意比例混溶,是因为与水形成氢键
- C、 IA族与VIIA族元素原子之间形成的化学键是离子键
- D、 同主族元素的简单阴离子还原性越强,水解程度越大
下列说法正确的是( )
- A、 氢氧燃料电池工作时,若消耗标准状况下11.2 L H2 , 则转移电子数为6.02×1023
- B、 常温下,将稀CH3COONa溶液加水稀释后,n(H+)﹒n(OH-)不变
- C、 合成氨生产中将NH3液化分离,可加快正反应速率,提高H2的转化率
- D、 反应2NaCl(s)=2Na(s)+Cl2(g)的ΔH<0,ΔS>0
25℃时,将amol/L、pH=m的一元酸HX溶液与bmol/L、pH=n的NaOH溶液等体积混合后pH>7。下列说法正确的是( )
- A、 若a=b,则HX一定是弱酸
- B、 反应后溶液中一定存在c(Na+)>c(X-)>c(OH-)>c(H+)
- C、 若a=b,则m+n<14
- D、 若a=2b,则反应后溶液中一定存在2c(OH-)=c(HX)+2c(H+)
下列说法中,正确的是( )
- A、 活化分子间的碰撞一定是有效碰撞
- B、 其他条件相同时,增大反应物浓度,反应物中活化分子的百分数增加
- C、 焓变和熵变都与反应的自发性有关,它们都能独立地作为自发性的判据
- D、 常温下,FeCl3溶液中由水电离出的c (H+)一定大于1×10﹣7mol/L
下列有关说法正确的是( )
- A、 镀锌铁制品镀层受损后,铁制品比受损前更容易生锈
- B、 2NaHCO3(s)=Na2CO3(s)+CO2(g)+H2O(l)室温下不能自发进行,说明该反应的△H<0
- C、 加热0.1 mol•L﹣1CH3COONa 溶液,CH3COO﹣的水解程度和溶液的pH均增大
- D、 N2(g)+3H2(g)⇌2NH3(g)△H<0,其他条件不变时升高温度,反应速率v(H2 )和H2的平衡转化率均增大