选择题

下列说法正确的是( )
- A、 曲线①代表
的沉淀溶解曲线
- B、 该温度下
的
值为
- C、 加适量
固体可使溶液由a点变到b点
- D、
时两溶液中

下列说法错误的是( )
- A、 L1代表-lgc(F-)与lg
的变化曲线
- B、 Ksp(SrF2)的数量级为10-9
- C、 a、c两点的溶液中均存在:2c(Sr2+)=c(F-)+c(HF)+c(Cl-)
- D、 c点的溶液中存在c(Cl-)>c(Sr2+)=c(HF)>c(H+)
实验现象 | 反应过程中的pH和电导率变化对比曲线 |
滴加氨水时,先不断产生浅蓝色沉淀;后来沉淀逐渐溶解,得到深蓝色溶液。 滴加硫酸时,先不断产生浅蓝色沉淀;后来沉淀逐渐溶解,得到蓝色溶液。 |
|
资料:ⅰ.实验中产生的浅蓝色沉淀为碱式硫酸铜,化学式为Cu2(OH)2SO4;
ⅱ.电导率是以数字表示的溶液中传导电流的能力。
下列分析中错误的是( )
- A、 a之前未加氨水,溶液pH<7的原因是Cu2++2H2O
Cu(OH)2+2H+
- B、 ab段发生的主要反应为:2Cu2++SO
+2NH3·H2O=Cu2(OH)2SO4↓+2NH
- C、 d点混合溶液pH<7,与反应后生成的NH
水解有关
- D、 根据a′b′与b′c′ 段曲线变化趋势,说明溶液的电导率仅与反应前后离子的浓度和离子所带电荷数有关

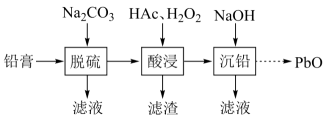
已知:ⅰ.铅膏的主要成分是和
;
是强酸;
ⅱ.、
。
下列有关说法错误的是( )
- A、 步骤②中反应
的化学平衡常数K约为
- B、 操作③需要用的玻璃仪器有烧杯、漏斗、玻璃棒
- C、 步骤④发生反应的离子方程式为
- D、 若步骤⑤用铅蓄电池作为电源电解
溶液,当电路中有
电子转移时,铅蓄电池负极质量的变化量与电解池阴极质量的变化量相等

- A、 曲线②代表CO
- B、 H2CO3的第二级电离常数为10-10.3
- C、 a=-4.35,b=-2.75
- D、 pH=10.3时,c(Ca2+)=10-7.6 mol·L-1
- A、 用臭氧进行自来水消毒
- B、 向酸性废水中加生石灰进行中和
- C、 用FeS除去工业废水中的Cu2+和Hg2+
- D、 用Na2SO4除去硬水中的Mg2+和Ca2+
实验1:向4 mL 0.01 mol·L-1AgNO3溶液中加入2 mL 0.01 mol·L-1NaCl溶液,产生白色沉淀。
实验2:向实验1所得悬浊液中加入2 mL0.01 mol·L-1NaBr溶液,产生淡黄色沉淀,过滤。
实验3:向实验2所得淡黄色沉淀中滴入一定量Na2S溶液,产生黑色沉淀,过滤。
已知:室温下Ksp(AgCl)=2×10-10。下列说法正确的是( )
- A、 实验1静置所得上层清液中c(Cl-)约为1.4×10 -5 mol·L-1
- B、 实验2的现象能够说明Ksp(AgCl)>Ksp(AgBr)
- C、 实验3所用Na2S溶液中存在c(OH-)=c(H+)+c(HS- )+c(H2S)
- D、 实验3过滤后所得清液中存在:c2(Ag+)=
且c(Ag+)≤

- A、 饱和BaCO3溶液中c(Ba2+)随pH增大而增大
- B、 BaCO3的溶度积Ksp=2.6×10-9
- C、 若忽略CO
的第二步水解,Ka2(H2CO3)=5×10-11
- D、 N点溶液中:c(Ba2+)>c(HCO
)>c(CO
)

下列对曲线的分析错误的是( )
- A、 ab段pH不断增大的原因是Mg(OH)2不断溶解导致的
- B、 bc段存在平衡Mg(OH)2(s)
Mg2+(sq)+2OH-(aq)
- C、 cd段中
- D、 通过实验数据对比可知,加入的稀硫酸的物质的量小于Mg(OH)2
- A、 NO遇空气变为红棕色:2NO+O2=2NO2
- B、 用NaOH溶液吸收Cl2:OH-+Cl2=HClO+Cl-
- C、 明矾净水:Al3++3H2O
Al(OH)3(胶体)+3H+
- D、 向AgI悬浊液中滴加Na2S溶液,沉淀变黑:2AgI(s)+S2-(aq)
Ag2S(s)+2I-(aq)
实验l:测得0.1mol·L-1H2S溶液pH=4.1
实验2:向10mL0.1mol·L-1NaHS溶液中加入5mL水,测得溶液的pH不断减小
实验3:向实验2所得溶液中滴加10mL0.1mol·L-1NaOH溶液,测得反应后溶液pH=12
实验4:向实验3所得溶液中滴加几滴0.1mol·L-1MnSO4溶液,产生粉色沉淀,再加几滴0.1mol·L-1CuSO4溶液,产生黑色沉淀
下列说法正确的是( )
- A、 由实验1可知:0.1mol·L-1H2S溶液中c(S2-)<c(OH-)
- B、 由实验2可知:加水过程中,
逐渐变小
- C、 实验3所得溶液中存在:c(H2S)+c(HS-)+c(H+)=c(OH-)
- D、 由实验4可知:Ksp(MnS)>Ksp(CuS)

- A、 L1代表-lgc(Sr2+)与
的变化曲线
- B、 Ksp(SrF2)的数量级为10-7
- C、 a、c两点的溶液中均存在2c(Sr2+)=c(F -)+c(HF)
- D、 c点的溶液中存在c(Cl-)< c(Sr2+)

已知:
I.As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
II.As2S3(s)+3S2-(aq)2AsS
(aq)
III.砷酸(H3AsO4)在酸性条件下有强氧化性,能被氢碘酸等还原
下列说法错误的是( )
- A、 As2S3中砷元素的化合价为+3价
- B、 “沉砷”过程中FeS可以用过量的Na2S代替
- C、 用氧气进行“氧化脱硫”涉及离子方程式AsS
+2O2=AsO
+3S↓
- D、 能用氢碘酸、淀粉溶液检验还原后溶液中是否仍存在砷酸

下列说法正确的是( )
- A、 曲线①代表
- B、
的数量级为
- C、 该温度下
与
为线性关系
- D、 溶液中始终存在

- A、 斜线③表示
随pH变化关系
- B、 该温度下,
时溶液的pH=9.3
- C、 根据图像不能计算该温度下CaCO3的
- D、 该温度下,H2CO3的电离平衡常数Ka1数量级为