选择题
用  盐酸滴定
盐酸滴定  溶液,溶液中
溶液,溶液中  、
、  、
、  的分布分数
的分布分数  随pH变化曲线及滴定曲线如图。下列说法正确的是(如
随pH变化曲线及滴定曲线如图。下列说法正确的是(如  分布分数:
分布分数:  )( )
)( )

- A、
的
为
- B、 c点:
- C、 第一次突变,可选酚酞作指示剂
- D、
下列操作规范且能达到实验目的的是( )
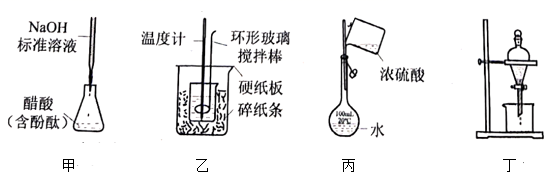
- A、 图甲测定醋酸浓度
- B、 图乙测定中和热
- C、 图丙稀释浓硫酸
- D、 图丁萃取分离碘水中的碘
25℃时,用1.0mol·L-1NaOH溶液滴定20.00mLc1mol·L-1的盐酸,用0.010mol·L-1NaOH溶液滴定20.00mLc2mol·L-1的盐酸,滴定曲线如图所示。下列说法错误的是( )

- A、 曲线a表示滴定c1mol·L-1的盐酸
- B、 c1:c2=100:1
- C、 滴定至pH=7时,两份溶液导电能力相同
- D、 水的电离程度在V(NaOH)=20.00mL时最大
室温下,向亚硫酸溶液中滴加NaOH溶液,各含硫微粒分布系数(平衡时某微粒的物质的量占各微粒物质的量之和的分数)与溶液pH的关系如图所示。下列说法不正确的是( )

- A、 曲线II表示HSO
的分布系数随pH的变化
- B、 Ka2(H2SO3)的数量级为10−8
- C、 pH=7时,c(Na+)<3c(SO
)
- D、 NaHSO3溶液中水电离出的c(H+)<1×10−7 mol·L−1
用0.1000mol/L的NaOH溶液分别滴定体积均为10.00mL、浓度均为0.1000mol/L的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液的电导率(电导率越大表示溶液导电性越强)变化如图所示.下列说法正确的是( )

- A、 曲线①代表向盐酸中滴加
- B、 A点溶液的
小于C点溶液的
- C、 D点溶液中:
- D、 随着
溶液的加入,曲线①逐渐向②靠拢,说明电解质溶液的电导率只与离子浓度大小相关
25℃时,用0.1mol·L-1NaOH溶液分别滴定20.00mL 0.1mol·L-1醋酸和20mL 0.1mol·L-1盐酸,滴定曲线如图所示,下列说法正确的是( )

- A、 a点所表示溶液中:c(H+)+c(CH3COOH)=c(OH-)+c(CH3COO-)
- B、 b点所表示溶液中:c(Cl-)>c(H+)>c(Na+)
- C、 Ka(CH3COOH)的数量级为10-6
- D、 溶液中水的电离程度:c>b>a
25℃时,向15mL0.1mol·L-1的NaOH溶液中逐滴滴入0.1mol·L-1的CH3COOH溶液,加入CH3COOH溶液的体积与混合溶液pH的关系如图所示(混合过程中忽略溶液体积变化)。下列分析不正确的是( )

- A、 c点对应溶液中,
=1
- B、 b点与c点所示溶液中水的电离程度:b>c
- C、 a点溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
- D、 b点对应的溶液中c(CH3COO-)+c(CH3COOH)=0.1mol·L-1
常温时,用0.1000mol·L-1 NaOH溶液滴定25.00mL 0.1000 mol·L-1一元弱酸HR的溶液,滴定过程中pH变化曲线如图所示(溶液体积近似可以加和),则下列判断正确的是( )

- A、 A点时,
- B、 常温下,HR的Ka的数量级为10-4
- C、 B点时,
- D、 B点和C点,水的电离程度相同
25℃时,向 溶液中逐滴滴入等浓度的
溶液中逐滴滴入等浓度的 溶液,测得溶液的
溶液,测得溶液的 与
与 [Y代表
[Y代表 或
或 ]的关系如图。下列相关结论正确的是( )
]的关系如图。下列相关结论正确的是( )

- A、 曲线a表示
与
的变化关系
- B、 25℃时
- C、 当溶液的
时,
- D、 当滴入
溶液时,
分析化学中“滴定分数”的定义为:所加滴定剂与被滴定组分的物质的量之比。常温下以0.10mol·L-1的HCl溶液滴定同浓度某一元碱MOH溶液并绘制滴定曲线如下图所示。下列说法不正确的是( )

- A、 该酸碱中和滴定过程应该选用甲基橙做指示剂
- B、 x点处的溶液中满足:c(MOH)+c(OH-)<c(M+)+c(H+)
- C、 根据y点坐标可以算得Kb(MOH)=9×10-7
- D、 从x点到z点,溶液中水的电离程度逐渐增大
用0.100mol/LNaOH溶液滴定20.00mLcmol/L二元酸H2A溶液,滴定曲线如图所示,下列叙述正确的是( )

- A、 HA—的电离常数的数量级是10-5
- B、 a点:c(HA-)>c (Na+)>c(H+)>c(A2-)>c(OH-)
- C、 b点:c(H+)=c(A2-)+c(OH-)
- D、 c点:c(Na+)<c(HA-)+2c(A2-)
羟胺的电离方程式为:NH2OH+H2O NH3OH+ + OH- , 用0.1 mol∙L−1的盐酸滴定20 mL0.1 mol∙L−1羟胺溶液,恒定25℃时,溶液AG与所加盐酸的体积( V)关系如图所示 [已知:AG
NH3OH+ + OH- , 用0.1 mol∙L−1的盐酸滴定20 mL0.1 mol∙L−1羟胺溶液,恒定25℃时,溶液AG与所加盐酸的体积( V)关系如图所示 [已知:AG ]。下列说法错误的是( )
]。下列说法错误的是( )

- A、 25℃时,羟胺的电离平衡常数Kb约为1.0×10−8
- B、 由c点到d点的过程中水的电离程度逐渐减小
- C、 图中b点V(盐酸)<10mL
- D、 d点对应溶液中存在c(H+) = c(OH-) + c(NH3OH+) + c(NH2OH)
用强碱滴定某一元弱酸时,弱酸被强碱部分中和后得到“弱酸盐和弱酸”组成的缓冲溶液,其中存在 。
。 时,用
时,用 的
的 溶液滴定
溶液滴定 某未知浓度的
某未知浓度的 溶液,滴定过程中消耗
溶液,滴定过程中消耗 溶液的体积与混合溶液
溶液的体积与混合溶液 之间的关系如图所示(已知:
之间的关系如图所示(已知: , 酸性
, 酸性 )。
)。

下列说法错误的是( )
- A、
电离常数的数量级为
- B、 b点溶液中存在
- C、 c点溶液中离子浓度的大小关系为
- D、 若将
改为等体积等浓度的
, 则
随
溶液体积的变化曲线竖直上移
用0.1000 的NaOH溶液滴定20.00mL浓度分别为c1、c2的醋酸、草酸(
的NaOH溶液滴定20.00mL浓度分别为c1、c2的醋酸、草酸( )溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点:
)溶液,得到如图滴定曲线,其中c、d为两种酸恰好完全中和的化学计量点:

下列叙述错误的是( )
- A、 X曲线代表草酸,Y曲线代表醋酸,
- B、 若b点时
, 则b点消耗了8.60mL的NaOH溶液
- C、 对于
而言,滴定过程中始终有
- D、 若a点
, 则a点有
常温下,向0.1mol/L HA溶液中逐渐加入NaOH固体,恢复至原温度后溶液中的关系如图所示(忽略溶液体积变化)。下列有关叙述正确的是( )

- A、 HA的Ka=l.0×104.65
- B、 A点溶液中:c(A-)+c(H+)+c(HA)-c(OH-)>0.1mol/L
- C、 B点溶液中:c(Na+)+c(H+)<c(OH-)+c(HA)
- D、 C点溶液中:c(A-)>c(Na+)>c(OH-)>c(H+)
室温下,向亚硫酸溶液中滴加NaOH溶液,各含硫微粒分布系数(平衡时某微粒的物质的量占各微粒物质的量之和的分数)与溶液pH的关系如图所示。下列说法错误的是( )

- A、 曲线II表示HSO
的分布系数随pH的变化
- B、 Ka2(H2SO3)的数量级为10−8
- C、 pH=7时,c(Na+)<3c(SO
)
- D、 NaHSO3溶液中水电离出的c(H+)<1×10−7 mol·L−1
25℃,分别取 一元酸HA、HB、HC,向其中逐滴滴入
一元酸HA、HB、HC,向其中逐滴滴入 溶液,并测出溶液pH随V(NaOH)/mL的变化如图。下列说法错误的是( )
溶液,并测出溶液pH随V(NaOH)/mL的变化如图。下列说法错误的是( )

- A、 反应完全后,若继续分别滴入NaOH溶液,溶液的pH主要取决于过量NaOH浓度
- B、 反应完全后,各混合液的pH均大于7
- C、 中和滴定实验中,HA被同浓度NaOH溶液滴定时误差最小
- D、 反应完全后,将三种溶液混合均匀:c(HA)+c(HB)+c(HC)+c(H+)+0.05=c(OH-)+c(Na+)
已知:  ,25℃时,
,25℃时,  的
的  ,
,  。用
。用  溶液滴定
溶液滴定  溶液的滴定曲线如图所示(曲线上的数字为pH)。下列说法正确的是( )
溶液的滴定曲线如图所示(曲线上的数字为pH)。下列说法正确的是( )

- A、 a点所得溶液中:
- B、 c点所得溶液中:
- C、 当溶液的pH为7时,此时加入NaOH溶液体积为30mL
- D、 随着NaOH溶液滴入,水的电离程度一直增大
常温下,用0.10 mol·L-1NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L-1CH3COOH溶液和HCN溶液,所得滴定曲线如图。下列说法错误的是( )

- A、 点①所示溶液中,CN-的水解程度大于HCN的电离程度
- B、 点①和点②所示溶液中:c(CN-)>c(CH3COO-)
- C、 点③所示溶液中:c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
- D、 点④所示溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
25℃时,Ka(CH3COOH)=1.7×10-5 , 该温度下,用0.1mol/L的醋酸溶液滴定10.00mL0.1mol/L的MOH溶液,滴定过程中加入醋酸溶液的体积(V)与溶液中lg  的关系如图所示,当V=0时,lg
的关系如图所示,当V=0时,lg  =-12。下列说法正确的是( )
=-12。下列说法正确的是( )

- A、 MOH是一元弱碱
- B、 a点:V(CH3COOH)=10.00mL
- C、 b点:c(CH3COOH)>c(M+)>c(H+)>c(OH-)
- D、 25℃时,CH3COO-的水解平衡常数约为5.9×10-10
水合乙二胺  是一种二元弱碱,在水中的电离方式与
是一种二元弱碱,在水中的电离方式与  相似,其
相似,其  .常温下,用
.常温下,用  盐酸滴定
盐酸滴定  乙二胺溶液.下列说法错误的是( )
乙二胺溶液.下列说法错误的是( )
- A、 乙二胺在水溶液中的第一步电离方程式为
- B、 滴定时选用酚酞作指示剂产生的误差最小
- C、 滴入
盐酸时,溶液呈碱性
- D、 滴入
盐酸时,加水稀释,溶液中
减小