单选题
化学与生活密切相关。下列说法错误的是( )
- A、 家庭储备的药品过期后应作为有害垃圾处理
- B、 食品包装袋里的硅胶颗粒可防止食品氧化变质
- C、 家用苏打可用于洗涤厨房用具的油污
- D、 铝制餐具不能长时间存放酸性或碱性食物
下列化学用语表示正确的是( )
- A、 用于考古断代的碳原子符号:
- B、 用电子式表示NaCl的形成过程:

- C、 乙酸乙酯的结构式:
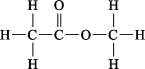
- D、 Ca2+的离子结构示意图:

下列说法正确的是( )
- A、 能电离出H+的化合物就是酸,能电离出OH-的化合物就是碱
- B、 金属氧化物都是碱性氧化物,非金属氧化物都是酸性氧化物
- C、 能导电的物质不一定是电解质,电解质不一定能导电
- D、 能否产生丁达尔效应是溶液和胶体的本质区别
某无色溶液中,下列离子可大量共存的是( )
- A、 K+、Ba2+、Cl-、
- B、 Cu2+、
、Na+、Br-
- C、 Mg2+、K+、
、
- D、 H+、Ca2+、
、I-
欲除去下列括号中的杂质,所选试剂正确的是( )
- A、 CO2(HCl)——饱和Na2CO3溶液
- B、 CH4(C2H4)——酸性KMnO4溶液
- C、 Cl2(HCl)——饱和食盐水
- D、 NH3(H2O)——浓硫酸
为了环境保护,工厂烟气可经过下列工艺进行脱硫,则2S(g)=S2(g)的反应热ΔH为( )
①H2S(g)+O2(g)=SO2(g)+H2O(g) ΔH1
②2H2S(g)+SO2(g)=S2(g)+2H2O(g) ΔH2
③H2S(g)+O2(g)=S(g)+H2O(g) ΔH3
- A、
ΔH1+ΔH2-ΔH3
- B、
ΔH1+
ΔH2-2ΔH3
- C、
ΔH1-
ΔH2+2ΔH3
- D、
ΔH1+
ΔH2-ΔH3
设NA为阿伏加德罗常数的值。下列说法错误的是( )
- A、 常温常压下,1.8gH2O含有NA个电子
- B、 1mol·L-1的CH3COONa溶液中,CH3COO-数目不一定小于NA
- C、 一定条件下,1mol金属钠与足量O2反应,转移NA个电子
- D、 标准状况下,22.4LSO3含有NA个分子
下列物质间的反应,反应物的用量或浓度不会影响生成物的是( )
- A、 NaHCO3和Ca(OH)2
- B、 Al2O3和NaOH溶液
- C、 Fe和稀HNO3
- D、 CO2和NaOH溶液
下列关于化学反应与能量的说法正确的是( )
- A、 NH4Cl固体和Ba(OH)2·8H2O反应时,反应物的总键能小于生成物的总键能
- B、 已知H2(g)+I2(g)
2HI(g) ΔH=-QkJ·mol-1 , 在一定条件下,向密闭容器中充入1molHI(g),反应达到平衡状态的过程中,吸收的热量为0.5QkJ
- C、 已知甲烷的燃烧热为890.3kJ·mol-1 , 则1mol甲烷充分燃烧生成CO2和水蒸气放出的热量小于890.3kJ
- D、 硫酸和盐酸分别与NaOH溶液反应的中和热数值之比为2:1
下列离子方程式书写正确的是( )
- A、 将少量CO2通入BaCl2溶液:CO2+Ba2++H2O=BaCO3↓+2H+
- B、 AlCl3溶液和氨水反应:Al3++3OH-=Al(OH)3↓
- C、 向NaClO溶液中通少量SO2:2ClO-+SO2+H2O=2HClO+
- D、 向盐酸中滴入少量Na2CO3溶液:
+2H+=CO2↑+H2O
实验室可用如图所示的装置制备SO2并探究其性质。下列说法错误的是( )

- A、 A装置中的药品可替换成铜片和浓硫酸
- B、 B装置可作储气瓶和安全瓶
- C、 C装置中溶液变浑浊,说明SO2具有氧化性
- D、 E中可选用NaOH溶液除去尾气
某些中草药中含有的咖啡酸具有止血的疗效,其结构简式如图所示。下列说法错误的是( )
![]()
- A、 该分子中所有原子不可能都共面
- B、 该物质可发生加成反应、酯化反应、取代反应
- C、 1mol该物质最多可与4molH2发生反应
- D、 该物质与Na、NaOH、Na2CO3均可反应
已知前四周期主族元素M、N、P、Q、W在周期表中的位置如图所示,且最外层电子数之和为20。则下列说法正确的是( )
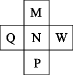
- A、 M、N的简单氢化物的稳定性:M<N
- B、 N、W的最高价氧化物对应的水化物酸性:N>W
- C、 Q是同周期主族元素中离子半径最小的元素
- D、 W的氯化物一定满足8电子稳定结构
下列离子浓度的关系正确的是( )
- A、 0.1mol·L-1K2S溶液中:c(H+)+c(HS-)+2c(H2S)=c(OH-)
- B、 0.1mol·L-1NaHCO3溶液中:c(
)+2c(
)+c(H2CO3)=c(Na+)
- C、 等物质的量的CH3COONa和盐酸的混合溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
- D、 物质的量浓度相等的NH4Cl溶液、CH3COONH4溶液和NH4HSO4溶液中c(
)依次增大
用海水得到的粗盐中含有较多杂质(如不溶性的泥沙,可溶性的CaCl2、MgCl2以及一些硫酸盐等),粗盐提纯的流程如图所示。下列说法错误的是( )
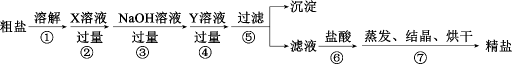
- A、 步骤①⑤⑦均会使用的仪器是玻璃棒
- B、 步骤②所加X溶液和步骤④所加Y溶液的顺序可以调换
- C、 步骤⑥加入盐酸的目的是除去过量的NaOH和Na2CO3
- D、 该提纯过程未涉及氧化还原反应
Fe2+催化H2O2分解产生HO•,HO•将NO氧化为 的机理如图所示,下列有关说法错误的是( )
的机理如图所示,下列有关说法错误的是( )
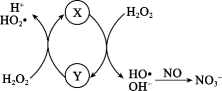
- A、 图中Y是Fe3+ , 是反应过程的中间产物
- B、 HO•将NO氧化为
的方程式为:3HO•+NO+OH-=
+2H2O
- C、 若反应温度过高,NO的去除率可能下降
- D、 图中H2O2均表现强氧化性
常温下,在不同试剂中加入酸或碱后体系pH的变化如表所示。下列说法错误的是( )
试剂 | pH | ||
初始 | 通入0.01molHCl气体 | 加入0.01molNaOH固体 | |
①1LH2O | 7 | a | 12 |
②0.10molCH3COOH,0.10molCH3COONa配制成1L的溶液 | 4.76 | 4.67 | 4.85 |
已知:缓冲作用是维持溶液自身pH值的相对稳定。
- A、 表中a的数值等于2(忽略通入HCl气体前后体系的体积变化)
- B、 试剂①如表所示通入HCl和加入NaOH相比,水的电离程度相同
- C、 试剂②中c(CH3COOH)>c(Na+)>c(CH3COO-)
- D、 NH3·H2O—NH4Cl溶液具有与试剂②相似的缓冲作用
爱迪生发明的镍铁碱性电池的寿命是铅蓄电池的数倍,为了纪念爱迪生的付出,这种电池也叫“爱迪生蓄电池”,其反应原理为:Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2 , 用爱迪生蓄电池制取少量Na2FeO4的装置如图所示。下列说法正确的是( )
Fe(OH)2+Ni(OH)2 , 用爱迪生蓄电池制取少量Na2FeO4的装置如图所示。下列说法正确的是( )
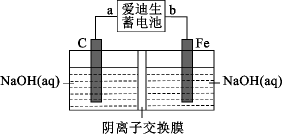
- A、 装置图中爱迪生蓄电池的负极是b
- B、 该电池工作一段时间充电时,生成NiO2的反应是还原反应
- C、 电解质溶液中OH-透过阴离子交换膜从右池移到左池
- D、 Fe电极上的反应为:Fe-6e-+8OH-=FeO
+4H2O
向某浓度的亚磷酸中滴加NaOH溶液,其pH与溶液中各种含磷微粒的物质的量分数 的变化如图所示。下列说法错误的是( )
的变化如图所示。下列说法错误的是( )
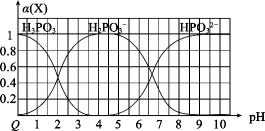
- A、 H3PO3是二元弱酸
- B、 该温度下,H3PO3的Ka1=1.0×10-2
- C、 NaH2PO3溶液显碱性
- D、 以酚酞为指示剂,当溶液由无色变为浅红色时,发生主要反应的离子方程式为:H2PO
+OH-=H2O+HPO