线上化学课堂中,老师演示了“吹气生火”实验,他向包有过氧化钠(Na
2O
2)粉末的脱脂棉上用导管吹气,脱脂棉燃烧了起来。同学们对该实验产生了浓厚兴趣,复学后进行了如下探究。
探究一:脱脂棉燃烧的原因。
(作出猜想)根据燃烧条件分析:①脱脂棉是可燃物;②吹出的气体可能与过氧化钠反应生成了氧气:③反应放出热量,满足了温度达到脱脂棉的。
(进行实验)在如图所示装置中,向过氧化钠粉末中不断吹气,观察到过氧化钠粉末由淡黄色逐渐变为白色,在导管口P处放置,木条复燃,说明试管内生成了氧气。同时还观察到,说明反应还放出了热量。
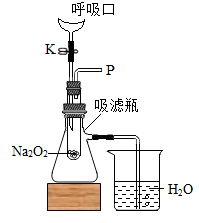
(得出结论)吹出的气体与过氧化钠反应生成了氧气,同时反应放出热量,满足了脱脂棉燃烧的条件。
探究二:试管内残留白色固体的成分。
(查阅资料)①吹出的气体主要成分有氮气、二氧化碳和水蒸气;
②过氧化钠与氮气不反应。
(作出猜想)猜想1:CO2参加反应,固体成分是Na2CO3;
猜想2:H2O参加反应,固体成分是NaOH;
猜想3:CO2和H2O均参加反应,固体成分是Na2CO3和NaOH。
(实验验证)
| 实验步骤 | 实验现象 | 实验结论 |
| ①取残留白色固体于试管中配成溶液,向其中加入足量的氯化钡溶液,静置 | 产生白色沉淀 | 固体成分含有碳酸钠 |
| ②取适量①的上层清液于试管中,向其中滴加少量氯化铜溶液 | 产生蓝色沉淀 | 固体成分含 |
(实验结论)过氧化钠与二氧化碳、水蒸气都能反应,猜想3正确。请写出过氧化钠与二氧化碳反应的化学方程式:。
(拓展延伸)化工厂存有过氧化钠时,一旦失火,不能选用(填字母序号)灭火。
A、二氧化碳灭火器
B、细沙
C、水基型灭火器