选择题
- A、 实验前试样未经干燥
- B、 试样中含有少量碳酸氢铵
- C、 试样中含有少量氯化钠
- D、 加热过程中有试样溅出来
实验目的 | 实验设计 | |
A. | 除去NaHCO3固体中的Na2CO3 | 将固体加热至恒重 |
B. | 制备无水AlCl3 | 蒸发Al与稀盐酸反应后的溶液 |
C. | 重结晶提纯苯甲酸 | 将粗品水溶、过滤、蒸发、结晶 |
D. | 鉴别NaBr和KI溶液 | 分别加新制氯水后,用CCl4萃取 |
- A、 A
- B、 B
- C、 C
- D、 D
下列制取SO2、验证其漂白性、收集并进行尾气处理的装置和原理能达到实验目的是( )
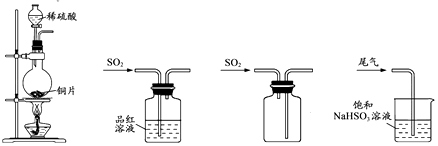
A B C D
- A、 制取SO2
- B、 验证漂白性
- C、 收集SO2
- D、 尾气处理
- A、 过滤操作中,漏斗的尖端应接触烧杯内壁
- B、 从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁
- C、 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
- D、 向容量瓶转移液体时,导流用玻璃棒可以接触容量瓶内壁
选项 | 试剂 | 试纸或试液 | 现象 | 结论 |
A | 浓氨水、生石灰 | 红色石蕊试纸 | 变蓝 | NH3为碱性气体 |
B | 浓盐酸、浓硫酸 | pH试纸 | 变红 | HCl为酸性气体 |
C | 浓盐酸、二氧化锰 | 淀粉碘化钾试液 | 变蓝 | Cl2具有氧化性 |
D | 亚硫酸钠、硫酸 | 品红试液 | 褪色 | SO2具有还原性 |
- A、 A
- B、 B
- C、 C
- D、 D
- A、 除去乙酸乙酯中的少量乙酸,可加入饱和碳酸钠溶液洗涤分液
- B、 在陶瓷坩埚中加强热,可除去碳酸钠晶体中的结晶水
- C、 实验室制取氢氧化铁胶体时,为了使胶体均匀应不断搅拌
- D、 用洁净的铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有Na+ , 无K+

- A、 图1模拟侯氏制碱法获得
- B、 图2用
溶液滴定未知浓度的醋酸溶液
- C、 图3
溶液,
, 探究温度对化学平衡的影响
- D、 图4探究苯酚和碳酸酸性强弱
选项 | 实验操作 | 现象 | 结论 |
A | 向某盐溶液中滴加几滴甲基橙溶液 | 溶液变红 | 该盐为强酸弱碱盐 |
B | 向NaCl、 | 有黑色沉淀生成 | |
C | 向酸性 | 溶液紫色褪去 |
|
D | 向浓硝酸中加入红热木炭 | 有红棕色气体生成 | 浓硝酸可与木炭发生反应 |
- A、 A
- B、 B
- C、 C
- D、 D
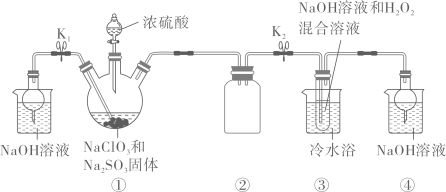
- A、 Na2SO3和H2O2均作还原剂
- B、 装置②,④的作用分别是防倒吸、吸收未反应的污染气体
- C、 从装置④反应后的溶液中获得晶体,可采用常压蒸发结晶
- D、 反应结束时,通氮气的目的是将仪器中残留的气体排入④中
|
|
|
|
A.制取并收集氨气 | B.从食盐水中提取 | C.用乙醇提取溴水中的溴 | D.牺牲阳极法保护铁 |
- A、 A
- B、 B
- C、 C
- D、 D
A.在铁制品上镀致密铜镀层 | B.探究浓度对反应速率的影响 | C.验证乙烯具有还原性 | D.制备FeSO4固体 |
|
|
|
|
- A、 A
- B、 B
- C、 C
- D、 D
实验 | 实验操作 | 实验现象 |
① | 分别向盛有少量FeS、Fe2S3固体的试管中加入稀盐酸 | 固体均溶解,均有臭鸡蛋气味气体生成;Fe2S3还有淡黄色浑浊生成 |
② | 向0.1mol/L FeCl3溶液中加入少量0.1 mol/L Na2S溶液 | 开始时,局部产生少量黑色沉淀,振荡,沉淀立即消失,同时有淡黄色浑浊和臭鸡蛋气味气体产生 |
③ | 向0.1 mol/L Na2S溶液中加入少量0.1 mol/L FeCl3溶液,产生现象后继续滴加足量盐酸 | 先有黑色沉淀生成,振荡沉淀不消失;滴加盐酸后,沉淀溶解,有淡黄色浑浊和臭鸡蛋气味气体生成 |
下列说法错误的是
- A、 配制 FeCl3溶液时,需将FeCl3固体溶于浓盐酸,再加水稀释至所需浓度
- B、 实验②中,沉淀消失发生反应的离子方程式为
- C、 由实验①、③中的现象可推知实验③中的黑色沉淀为Fe2S3
- D、 FeCl3溶液与Na2S溶液反应的产物与反应体系的酸碱性有关
- A、 用稀硝酸清洗试管内壁的银镜
- B、 用带橡胶塞的棕色细口瓶保存溴水
- C、 用玻璃棒蘸取样品进行焰色试验
- D、 用pH试纸测定过氧乙酸溶液的pH

- A、 装置甲:明矾晶体制备KAl(SO4)2
- B、 装置乙:制备少量干燥的NH3
- C、 装置丙:常温下分离苯酚与水的混合物
- D、 装置丁:探究浓度对化学反应速率的影响








 ),溶液变为橙红色,然后再加入酸,溶液颜色变浅(与加入等量水比较)
),溶液变为橙红色,然后再加入酸,溶液颜色变浅(与加入等量水比较)







 )是一种重要的化工原料,一种由H2O2氧化环己醇制备环己酮的实验方法如下:
)是一种重要的化工原料,一种由H2O2氧化环己醇制备环己酮的实验方法如下: 
